Traitement
Pour les dermatoses auto-immunes ou à médiation immune, deux approches thérapeutiques peuvent être utilisées : l’immunosuppression ou l’immunomodulation (Tableau 1a, b et c). Le type et la sévérité de la maladie déterminent l’approche la plus appropriée. La majorité des chiens souffrant de lupus érythémateux discoïde, de vascularite cutanée induite par la vaccination antirabique, de vascularite du bord libre des pavillons auriculaires, et d’onychodystrophie lupoïde symétrique répondent favorablement et peuvent être contrôlés grâce aux immuno-modulateurs. D’autres maladies telles que le pemphigus foliacé, l’érythème polymorphe, le lupus érythémateux systémique et d’autres formes de vascularite nécessitent un recours aux immunosuppresseurs.
Tableau 1a. Médicaments couramment utilisés dans le traitement des dermatoses auto-immunes et à médiation immune 1,24,25
Les immunomodulateurs exercent, le plus souvent, leur effet en 3 à 4 semaines. Si les signes cliniques sont sévères, une corticothérapie initialement prescrite à forte dose puis progressivement diminuée peut y être associée pour contrôler rapidement les symptômes. Une fois la rémission observée, l’immunomodulateur pourra être conservé seul en entretien. Le principal bénéfice des immunomodulateurs est qu’ils ont moins d’effets secondaires et de répercussions sur l’état général, notamment à long terme.
Les immunosuppresseurs le plus utilisés sont les corticoïdes. Initialement, des doses élevées sont nécessaires pour obtenir une rémission. Elles sont ensuite diminuées progressivement jusqu’à trouver la plus petite dose efficace. Pour de nombreuses maladies auto-immunes, des traitements adjuvants sont nécessaires pour arriver à réduire suffisamment la dose de corticoïdes pour limiter leurs effets secondaires. Dans les cas sévères, il n’est pas rare de devoir associer différents immunosuppresseurs pour obtenir et maintenir la rémission. Les autres immunosuppresseurs incluent l’azathioprine, la ciclosporine, le mycophénolate mofétil, le cyclophosphamide et le chlorambucil. Comme beaucoup de ces médicaments peuvent avoir des effets indésirables sur le foie et la moelle osseuse, il est recommandé d’effectuer un bilan sanguin toutes les 2-3 semaines pendant les premiers mois, puis tous les 4 à 6 mois en entretien. Si les paramètres sanguins montrent des variations significatives, le médicament en cause devra être arrêté et remplacé par un autre produit. L’utilisation d’immunoglobulines intraveineuses humaines (hIVIg) a montré des résultats prometteurs pour le traitement des dermatoses auto-immunes sévères lors d’échec des autres traitements 6. Des traitements adjuvants tels que des traitements symptomatiques lors de plaies ouvertes, une fluidothérapie et un soutien nutritionnel peuvent se révéler nécessaires dans certains cas.
Lors de lésions localisées ou pour contrôler une poussée, le recours aux traitements topiques ne doit pas être négligé. Un dermocorticoïde tel que la bétaméthasone a l’avantage d’offrir un contrôle rapide de l’inflammation et des lésions, mais son utilisation prolongée risque d’induire une atrophie cutanée. Le tacrolimus peut être une alternative mieux tolérée sur le long terme.
Tableau 1b. Médicaments couramment utilisés dans le traitement des dermatoses auto-immunes et à médiation immune 1,24,25
Quatre phases sont à considérer dans le traitement des dermatoses auto-immunes : la phase d’induction, la phase de transition, la phase d’entretien et la détermination de la guérison permettant l’arrêt du traitement 1. En phase d’induction, l’objectif est de stopper le processus inflammatoire le plus rapidement possible et de supprimer la réaction immunitaire dirigée contre la peau. Dans cette phase, des doses élevées de médicaments sont habituellement nécessaires. En l’absence de réponse satisfaisante dans un délai raisonnable, un autre protocole de traitement devra être envisagé, c’est-à-dire qu’il faudra remplacer les médicaments en cours par d’autres médicaments ou en rajouter. En phase de transition, les doses de médicaments sont diminuées pour limiter les effets secondaires. En cas d’association de plusieurs médicaments, il faudra réduire en premier ceux dont les effets secondaires sont les plus importants (corticoïdes, par exemple). Les doses sont diminuées progressivement, souvent sur plusieurs semaines, voire plusieurs mois, jusqu’à atteindre la plus petite dose efficace (phase d’entretien). Les diminutions de dose sont effectuées par paliers progressifs. En cas de réapparition des signes cliniques lors du passage à un palier, les doses de médicaments sont ré-augmentées au palier précédent jusqu’à l’obtention d’une nouvelle rémission, puis rediminuées plus progressivement. La « guérison » est déterminée, pour les dermatoses à médiation immune, par l’obtention d’une rémission et une absence de récidive suite à l’arrêt du traitement.
L’arrêt du traitement d’entretien chez un animal bien contrôlé est une décision difficile à prendre, surtout si les signes initiaux étaient sévères. Cette décision doit être prise en accord avec le propriétaire. Il est essentiel que le client soit bien informé et qu’il ait conscience qu’en cas de rechute, une nouvelle rémission risque d’être plus difficile à obtenir. Le bon moment pour arrêter dépend du type de la maladie, du fait qu’un facteur déclenchant ait été identifié et éliminé, et du risque vital encouru par l’animal. Dans de nombreux cas, le traitement d’entretien doit être administré pendant au moins 8 à 12 mois 1. avant d’envisager son arrêt.
Il est souvent déconseillé de continuer à vacciner les animaux souffrant de dermatoses auto-immunes, même ceux chez qui la vaccination n’est pas un facteur déclenchant reconnu. Cette précaution repose sur l’idée que la vaccination risque de stimuler une réponse immunitaire non spécifique, pouvant induire une recrudescence de la maladie auto-immune 7. L’auteur préfère suspendre la vaccination antirabique et contrôler régulièrement les titres d’anticorps contre la maladie de Carré et la parvovirose. Si les titres sont insuffisants pour maintenir une bonne immunité, le rapport bénéfice/risque doit être évalué au cas par cas.
Tableau 1c. Médicaments couramment utilisés dans le traitement des dermatoses auto-immunes et à médiation immune 1,24,25
Maladies spécifiques
Pemphigus foliacé
Il s’agit de la dermatite auto-immune la plus fréquente chez le chien, se traduisant par une atteinte pustulo-croûteuse. Cette maladie affecte l’épiderme, en ciblant différentes molécules d’adhésion, notamment celles composant les desmosomes qui assurent la cohésion des kératinocytes. Chez l’Homme souffrant de pemphigus foliacé, la desmogléine-1 (DSG1), une glycoprotéine desmosomiale, est la principale cible des auto-anticorps 8 ; elle a également été suspectée d’être la cible principale chez le chien 9,10. Toutefois, il semblerait qu’elle ne soit en réalité qu’un auto-antigène mineur dans cette espèce 11, la desmocolline-1 étant la cible la plus probable 12.
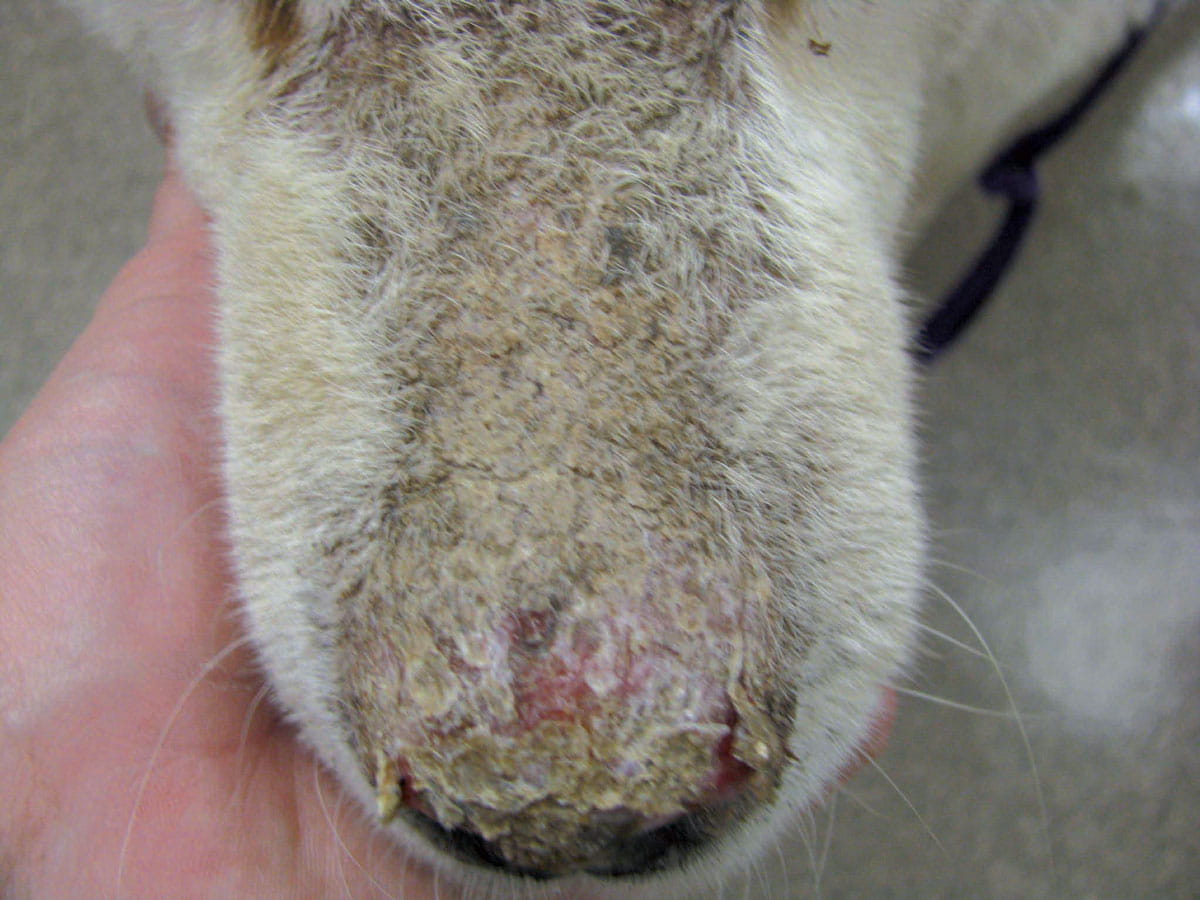
Des facteurs génétiques semblent jouer un rôle dans le développement de la maladie, les races Akita Inu et Chow Chow étant surreprésentées 10. Parmi les facteurs déclenchants, citons les allergies cutanées, les médicaments (antibiotiques, AINS, antiparasitaires), mais surtout les rayons UV 1,10. La lésion initiale est une macule évoluant rapidement en pustules, de grande taille le plus souvent et coalescentes. Les pustules sont souvent fragiles et se rompent facilement, entraînant la formation de croûtes. Ainsi, les croûtes sont le signe clinique le plus fréquent 1,9,10. Des érosions peuvent être visibles. Les ulcérations sont rares mais peuvent être présentes dans les cas compliqués de pyodermite profonde. Le pemphigus foliacé canin est souvent caractérisé par des croûtes, initialement localisées à la face (notamment le chanfrein et la truffe, la région péri-oculaire et les pavillons auriculaires), avec évolution vers une forme généralisée (Figure 2).
La cytologie d’une pustule intacte ou de la peau sous une croûte révèle souvent la présence de nombreux neutrophiles non dégénérés entourant des kératinocytes acantholytiques isolés ou en grappes, ayant l’aspect de grands kératinocytes basophiles nucléés arrondis (Figure 1). L’examen histologique révèle des pustules sous-cornées contenant des neutrophiles avec plus ou moins d’éosinophiles, et des kératinocytes acantholytiques 13. Le traitement implique souvent des doses élevées de corticoïdes associées à un autre immunosuppresseur et des topiques.
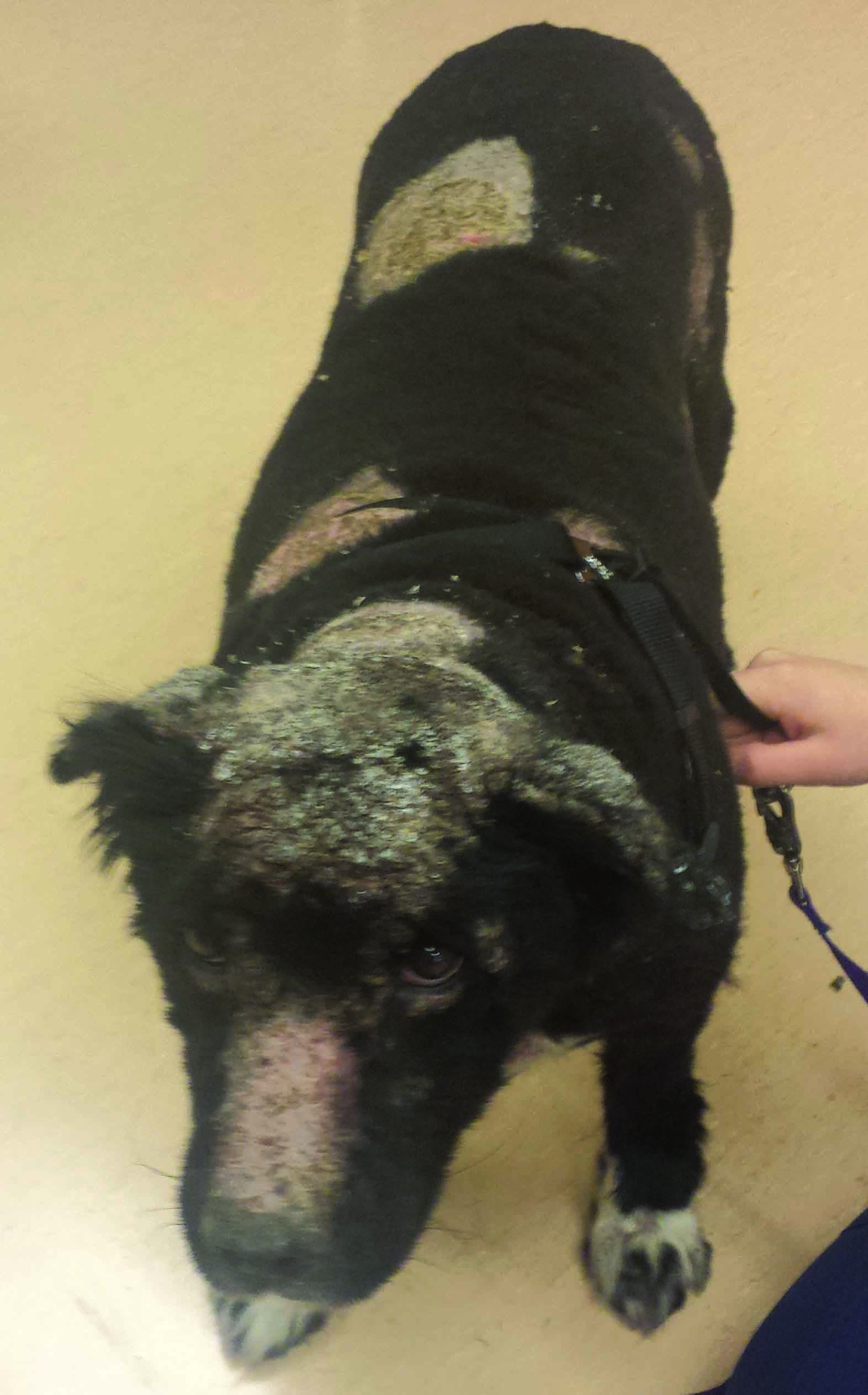
Figure 2. Pemphigus foliacé : (a) croûtes mélicériques localisées au chanfrein et à la truffe. Érosions légères de la truffe visibles sous les croûtes soulevées. (b) Tableau clinique plus généralisé de pemphigus foliacé.
© Amy Shumaker
Lupus érythémateux discoïde
Également appelé « nez de Colley » ou lupus érythémateux cutané, le lupus érythémateux discoïde est une maladie ulcérative bénigne sans signes systémiques 1. Ce lupus est généralement localisé à la truffe, mais peut aussi toucher les zones exposées au soleil des pavillons auriculaires et du pourtour des yeux, et il existe des cas décrits de variante généralisée 14. Le signe clinique le plus fréquent est la perte initiale des dermatoglyphes de la truffe, évoluant vers une dépigmentation et une desquamation (Figure 3). Avec la chronicité, des érosions, ulcérations et croûtes apparaissent. Des plaques hyperpigmentées annulaires à polycycliques localisées au cou, au tronc et aux extrémités peuvent s’observer dans les cas de variante généralisée.
L’histopathologie révèle une dégénérescence (apoptose) des cellules basales de l’épiderme, avec infiltrat lichénoïde polycellulaire modéré du derme 13. Cette maladie pouvant mimer cliniquement et histopathologiquement une pyodermite cutanéo-muqueuse, l’évaluation cytologique via la réalisation d’un calque cutané sous-crustacé sur la truffe peut se révéler utile. Une antibiothérapie est recommandée si des bactéries sont observées. Dans la majorité des cas de lupus érythémateux discoïde, il est inutile d’utiliser des immunosuppresseurs puissants. Une approche immunomodulatrice systémique associant une tétracycline (doxycycline, minocycline) au nicotinamide, parallèlement à un traitement topique (dermocorticoïdes, tacrolimus), permet souvent de contrôler efficacement la maladie. Dans les cas réfractaires ou sévères, des doses élevées de corticoïdes peuvent être initialement nécessaires. Dans les cas décrits de variante généralisée, l’hydroxychloroquine ou la ciclosporine ont été utilisées avec succès 14,15. Les rayons UV jouant un rôle significatif dans la maladie, il est important de limiter au maximum l’exposition au soleil et d’utiliser des crèmes solaires. Une supplémentation en vitamine E (400 UI par jour) peut également se révéler utile.