Behandlung
Bei autoimmunen/immunvermittelten Dermatosen werden zwei therapeutische Strategien unterschieden: Immunsuppression und Immunmodulation (Tabelle 1a, b und c). Welche Strategie im Einzelfall zum Einsatz kommt, wird in erster Linie durch den Erkrankungstyp und den Grad der Erkrankung bestimmt. Die meisten Hunde mit diskoidem Lupus erythematosus, Tollwutvakzine-induzierter kutaner Vaskulitis, Vaskulitis der Ohrränder und symmetrischer lupoider Onychodystrophie sprechen gut auf immunmodulatorische Arzneimittel an und können mit einer entsprechenden Behandlung stabil gehalten werden. Andere Erkrankungen wie Pemphigus foliaceus, Erythema multiforme, systemischer Lupus und verschiedene andere Vaskularitiden erfordern dagegen immunsuppressive Behandlungen.
Tabelle 1a. Häufig eingesetzte Arzneimittel für die Behandlung autoimmuner und immunvermittelter Hauterkrankungen 1,24,25
Immunmodulatorische Arzneimittel können einige Zeit benötigen, um eine erkennbare Besserung zu bewirken (im Allgemeinen 3-4 Wochen). Bei Patienten mit hochgradigen Symptomen kann daher initial mit hochdosierten Glucocorticoiden in ausschleichender Dosierung behandelt werden, um eine schnelle klinische Kontrolle der Erkrankung zu erreichen, zusammen mit dem gewählten immunmodulatorischen Arzneimittel. Sobald eine Remission erreicht ist, kann das immunmodulatorische Arzneimittel allein als Erhaltungstherapie fortgesetzt werden. Zu beachten ist, dass initial sowohl Glucocorticoide als auch begleitend das immunmodulatorische Arzneimittel verabreicht werden sollten, da Letzteres eine gewissen Zeit benötigt, um seine Wirkung zu entwickeln. Dadurch verhindert man die Entstehung von Rezidiven während des Ausschleichens der Steroide. Hauptvorteil immunmodulatorischer Arzneimittel ist, dass sie weniger hochgradige Nebenwirkungen haben als Immunsuppressiva und zu einer geringeren Beeinträchtigung der Gesundheit des Patienten führen.
Für die immunsuppressive Therapie werden am häufigsten Glucocorticoide eingesetzt. Initial sind meist hohe Dosen erforderlich, um eine Remission zu erreichen. Anschließend wird die Dosierung ausgeschlichen bis zur niedrigsten wirksamen Dosis, mit der die Remission bei minimalen systemischen Effekten noch aufrechterhalten werden kann. Bei vielen Autoimmunkrankheiten sind jedoch adjunktive Behandlungen notwendig, um die Glucocorticoiddosis auf ein Niveau absenken zu können, das Nebenwirkungen weitgehend minimiert. In sehr hochgradigen Fällen werden nicht selten mehrere immunsuppressive Arzneimittel kombiniert eingesetzt, um eine Remission zu erreichen und aufrechtzuerhalten. Da jedoch viele dieser Arzneimittel potenzielle Nebenwirkungen im Bereich der Leber und des Knochenmarks haben, wird eine kontinuierliche Überwachung der Blutwerte alle 2-3 Wochen über die ersten Monate der Behandlung und anschließend regelmäßig alle 4-6 Monate empfohlen. Wenn signifikante Veränderungen von Blutparametern festgestellt werden, sollte das verursachende Arzneimittel abgesetzt und durch ein anderes ersetzt werden. Die am häufigsten eingesetzten adjunktiven Arzneimittel sind Azathioprin, Cyclosporin, Mycophenolatmofetil, Cyclophosphamid und Chlorambucil. Bei höhergradig betroffenen Hunden können eine unterstützende Therapie zur Behandlung offener Wunden, eine korrektive Flüssigkeitstherapie und eine regelmäßige Überwachung der Serumproteinkonzentration erforderlich sein. Der Einsatz von humanem intravenösem Immunglobulin (hIVIg) zeigt Untersuchungen zufolge vielversprechende Ergebnisse bei der Behandlung hochgradiger autoimmuner Dermatosen, wenn andere Behandlungen scheitern 6.
Topische Behandlungen können bei eher lokal begrenzten oder sporadisch aufblühenden Effloreszenzen hilfreich sein. Am häufigsten zum Einsatz kommen Präparate mit Betamethason oder Tacrolimus. Der Vorteil von Betamethason liegt in der schnellen Kontrolle des Entzündungsgeschehens und der Krankheitssymptome. Ein Nachteil ist jedoch die mögliche Induzierung einer dermalen Atrophie bei längerer Anwendung. Wenn eine topische Langzeitbehandlung erforderlich ist, sollte deshalb eine Umstellung auf Tacrolimus erfolgen.
Tabelle 1b. Häufig eingesetzte Arzneimittel für die Behandlung autoimmuner und immunvermittelter Hauterkrankungen 1,24,25
Bei der Behandlung autoimmuner Dermatosen werden vier Phasen unterschieden: Einleitungsphase, Umstellungsphase, Erhaltungsphase und Bestimmung der Heilung 1. In der Einleitungsphase sind die therapeutischen Ziele das schnellstmögliche Stoppen der entzündlichen Komponente und die Suppression der gegen die Haut gerichteten immunologischen Reaktionen. In der Regel sind in dieser ersten Phase höhere Arzneimitteldosen erforderlich. Kann ein akzeptables Ansprechen nicht zeitnah erreicht werden, sollte eine Umstellung der Behandlung in Betracht gezogen werden, also entweder alternative Arzneimittel oder zusätzliche Arzneimittel zum aktuellen Behandlungsregime. In der anschließenden Umstellungsphase werden die eingesetzten Arzneimittel ausgeschlichen, um Nebenwirkungen und unerwünschte Ereignisse zu minimieren. Bei medikamentösen Kombinationsbehandlungen werden an erster Stelle die Arzneimittel mit den stärksten Nebenwirkungen – wie z. B. Glucocorticoide – ausgeschlichen. Das Ausschleichen erfolgt langsam, oft über mehrere Wochen oder Monate, bis eine akzeptable Erhaltungsdosis erreicht ist oder die Symptome rezidivieren. Im letzteren Fall wird die Medikation wieder bis zum Erreichen einer erneuten Remission erhöht und dann wieder ausgeschlichen bis zur letzten Dosis, die noch in der Lage ist, die Symptome des Patienten unter akzeptabler Kontrolle zu halten (Erhaltungsphase). Von einer „Heilung“ spricht man bei Patienten mit immunvermittelter Dermatose dann, wenn eine Remission erreicht wurde, die Symptome mit einer Erhaltungstherapie erfolgreich unter Kontrolle gehalten werden und nach dem Absetzen nicht wieder rezidivieren.
Das Absetzen einer erfolgreichen Erhaltungstherapie bei einem Patienten mit gut kontrollierter Erkrankung ist immer eine schwierige Entscheidung, insbesondere, wenn die initiale Erkrankung sehr hochgradig war. Eine solche Entscheidung sollte deshalb stets im gegenseitigen Einvernehmen zwischen Tierarzt und Besitzer erfolgen. Der Besitzer muss deutlich darüber aufgeklärt werden, dass eine erneute Remission im Falle eines Rezidivs in diesen Fällen schwieriger zu erreichen sein kann, als bei der erstmaligen Behandlung. Der Zeitpunkt des Absetzens einer Erhaltungstherapie richtet sich nach dem Typ der Erkrankung, nach der Frage, ob ein Auslöser identifiziert und ausgeschaltet werden konnte, und nach der Einschätzung des Risikos für den Patienten, wenn die Behandlung nicht fortgesetzt wird. In vielen Fällen wird eine Erhaltungstherapie über eine Dauer von acht bis zwölf Monaten empfohlen 1. Bei Tieren, bei denen das Rezidivrisiko die Vorteile eines Absetzens der Behandlung überwiegt, kann die medikamentöse Therapie unter geeigneter labordiagnostischer Überwachung auch lebenslang fortgesetzt werden.
Vor zukünftigen Impfungen wird bei Patienten mit Autoimmundermatosen oft abgeraten, und zwar selbst dann, wenn die Impfung im Einzelfall gar nicht als Auslöser identifiziert werden konnte. Begründet wird dies mit der Sorge, dass Impfungen generell eine breite, unspezifische Immunantwort induzieren können, die möglicherweise ein Rezidiv der Autoimmunerkrankung hervorrufen 7. Die Autorin zieht es vor, Tollwutimpfungen vollständig auszusetzen, und die Staupe- und Parvovirustiter regelmäßig zu überwachen. Sind diese Titer nicht ausreichend hoch, um eine wirksame Immunität aufrechtzuerhalten, sollte vor der erneuten Impfung in jedem Fall zunächst eine individuelle Risiko-Nutzen-Abwägung erfolgen.
Tabelle 1c. Häufig eingesetzte Arzneimittel für die Behandlung autoimmuner und immunvermittelter Hauterkrankungen 1,24,25
Spezifische Erkrankungen
Pemphigus foliaceus
Die häufigste autoimmune Hauterkrankung bei Hunden ist der Pemphigus foliaceus (PF). Es handelt sich um eine pustuläre bis krustöse autoimmune Dermatitis. Pemphigus foliaceus betrifft die Epidermis und attackiert verschiedene Adhäsionsmoleküle, insbesondere Desmosomen, die für den Zusammenhalt von Keratinozyten verantwortlich sind. Beim humanen Pemphigus foliaceus ist das Hauptangriffsziel der Autoantikörper das Desmoglein-1-Glycoprotein (DSG1) in den Desmosomen 8. Dasselbe Glycoprotein wurde in der Vergangenheit auch als Hauptangriffsziel bei Hunden betrachtet 9,10. Heute geht man jedoch davon aus, dass es sich hierbei um ein weniger wichtiges Autoantigen handelt 11. Neuere Evidenzen legen nahe, dass Desmocollin-1 ein wichtiges Autoantigen beim Pemphigus foliaceus des Hundes ist 12.
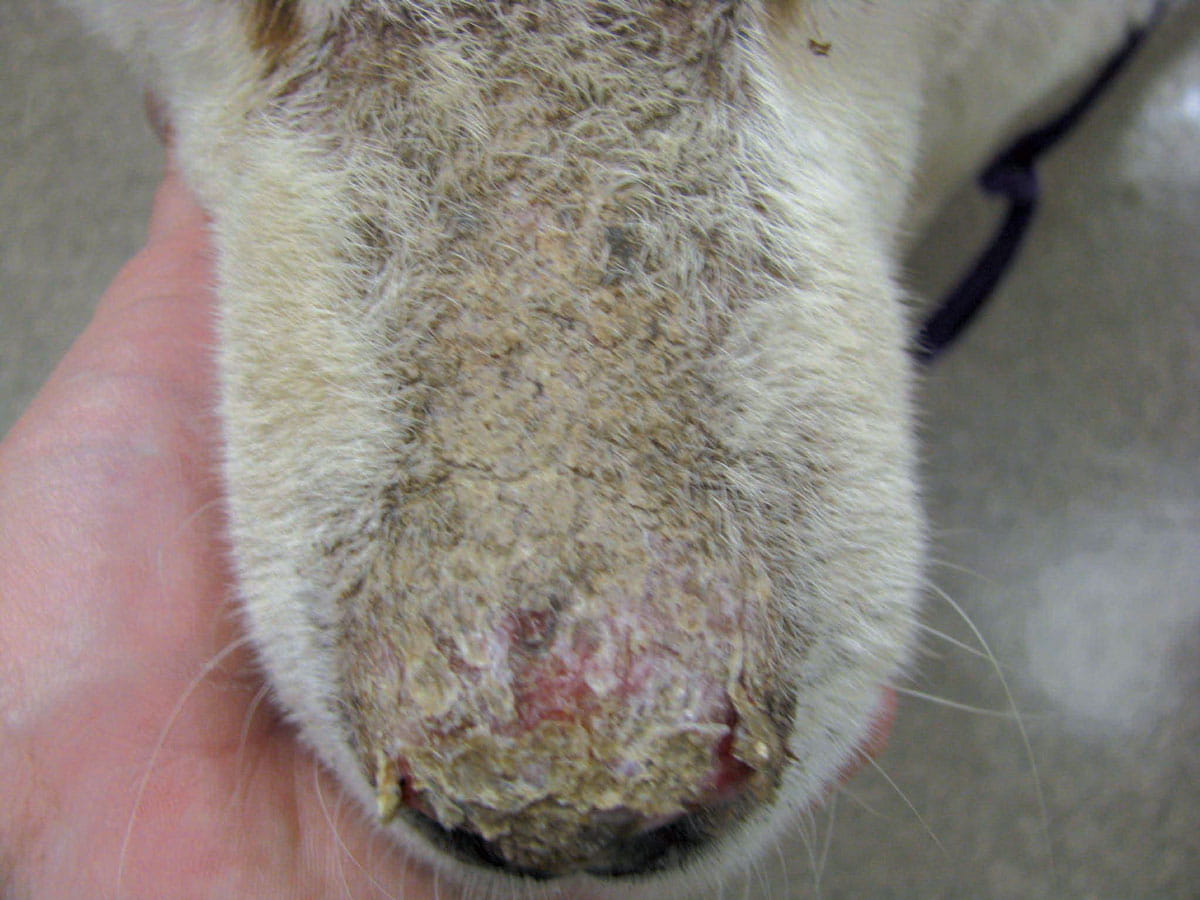
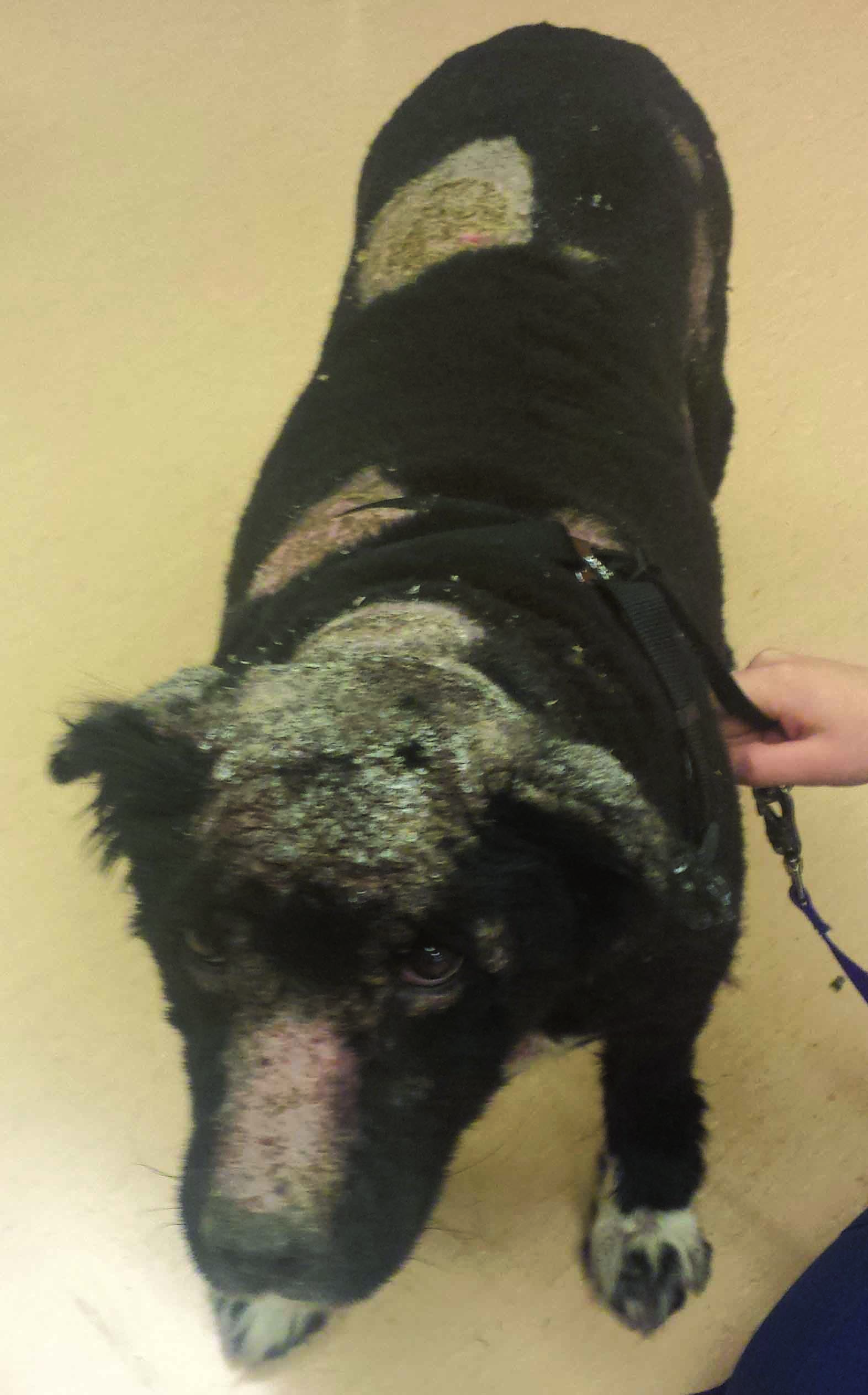
Auch genetische Faktoren scheinen eine Rolle bei der Entwicklung des Pemphigus foliaceus zu spielen, wobei Akitas und Chow-Chows als die Rassen mit dem höchsten Risiko gelten 10. Potenzielle Auslöser eines Pemphigus foliaceus sind chronische allergische Hauterkrankungen und Arzneimittel (Antibiotika, NSAIDs, topische Spot-on-Präparate gegen Flöhe), der wichtigste auslösende Faktor ist jedoch ultraviolettes Licht 1,10. Die initialen Effloreszenzen sind Makulae, die schnell zu Pusteln fortschreiten, die oft groß und zusammenfließend sind. Die Pusteln sind häufig sehr fragil, rupturieren leicht und führen so zu Krustenbildung, dem häufigsten klinischen Symptom bei Pemphigus foliaceus 1,9,10. Auch Erosionen können festzustellen sein, während Ulzera zwar eher selten vorkommen, in Fällen, die durch eine tiefe Pyodermie kompliziert werden, aber durchaus zu beobachten sein können. Pemphigus foliaceus ist bei Hunden oft gekennzeichnet durch eine Krustenbildung, die initial den Gesichtsbereich betrifft (insbesondere Nasenrücken und Nasenspiegel, die periokuläre Region und die Ohrmuscheln) und im weiteren Verlauf zu einer generalisierten Form fortschreitet (Abbildung 2).
Die zytologische Untersuchung einer intakten Pustel oder der Haut unter einer Kruste zeigt oft zahlreiche nicht-degenerierte neutrophile Granulozyten, die einzelne oder in Clustern angeordnete, akantholytische Keratinozyten umgeben, die sich als große, runde, basophile, kernhaltige Zellen darstellen (Abbildung 1). Die histologische Untersuchung zeigt subkorneale Pusteln, die neutrophile Granulozyten, variable Anzahlen eosinophiler Granulozyten und akantholytische Keratinozyten enthalten 13. Die Behandlung erfolgt oft mit hochdosierten Steroiden und einem adjunktiven Immunsuppressivum, sowie topischen Präparaten für die lokale Behandlung.
Abbildung 2. Pemphigus foliaceus: (a) Honigfarbene Verkrustungen am Nasenrücken und Nasenspiegel. Unter den angehobenen Krusten erkennt man eine geringgradige Erosion des Nasenspiegels. (b) Generalisiertere Form des Pemphigus foliaceus.
© Amy Shumaker
Discoider Lupus erythematosus
Bei dem auch als „Collie Nose“ oder kutaner Lupus erythematosus bezeichneten discoiden Lupus erythematosus (DLE) handelt es sich um eine benigne ulzeröse Erkrankung ohne systemische Manifestation 1. DLE entsteht im Allgemeinen am Nasenspiegel, kann aber auch die sonnenlicht-exponierten Bereiche der Ohrmuscheln und die periokuläre Region betreffen, und einigen Berichten zufolge auch in einer generalisierten Variante auftreten 14. Das häufigste klinische Symptom ist ein initialer Verlust der pflastersteinartigen Architektur des Nasenspiegels, der zu Depigmentierung und schuppiger Abschilferung fortschreitet (Abbildung 3). Bei chronischen Verläufen bilden sich Erosionen, Ulzera und Krusten. In generalisierten Fällen können kreisförmige bis polyzyklische hyperpigmentierte Plaques am Hals, am Stamm und an den Extremitäten zu beobachten sein.
Die Histopathologie zeigt eine Interface-Basalzelldegeneration (Apoptose) mit einer moderaten pleozellulären lichenoiden Infiltration der Dermis 13. Da diese Erkrankung der mukokutanen Pyodermie sowohl unter klinischen als auch unter histopathologischen Aspekten sehr ähnlich ist, kann eine zytologische Untersuchung von Probenmaterial unter einer Kruste auf dem Nasenspiegel sehr hilfreich sein. Wenn Bakterien nachgewiesen werden, ist eine antibiotische Behandlung gegen die mukokutane Pyodermie zu empfehlen. In den meisten Fällen eines DLE ist eine Behandlung mit potenten Immunsuppressiva nicht erforderlich. Oft lässt sich die Erkrankung durch eine systemische immunmodulatorische Therapie mit Tetracyclin (Doxycyclin, Minocyclin) und Niacinamid, kombiniert mit einer topischen Behandlung (topische Steroide, Tacrolimus) erfolgreich unter Kontrolle bringen. In therapieresistenten oder hochgradigen Fällen können initial jedoch hochdosierte Corticosteroide erforderlich sein. Bei den in der Literatur beschriebenen generalisierten Varianten erwiesen sich Hydroxychloroquin oder Cyclosporin als wirksame Behandlungsoptionen 14,15. Da Sonnenlicht eine wichtige Rolle bei der Entstehung des DLE spielt, müssen betroffene Patienten durch Vermeiden von Sonnenlicht und die Anwendung von Sonnenschutzmitteln geschützt werden. Eine Vitamin-E-Supplementierung (400 IE täglich) kann die Behandlung unterstützen.