Tratamiento
Existen dos enfoques para el tratamiento de las dermatosis autoinmunes e inmunomediadas: la inmunosupresión o la inmunomodulación (Tabla 1a, b y c). El tipo y la gravedad de la enfermedad determinan el enfoque que se debe seguir.
La mayoría de los perros con lupus eritematoso discoide, vasculitis cutánea inducida por la vacuna de la rabia, vasculitis del margen auricular y onicodistrofia lupoide simétrica se pueden tratar con fármacos inmunomoduladores. Otras enfermedades como el pénfigo foliáceo, eritema multiforme, lupus sistémico y otras vasculitis pueden tratarse con fármacos inmunosupresores.
Tabla 1a. Fármacos frecuentes en el tratamiento de las dermatosis autoinmunes e inmunomediadas 1,24,25
*Los comprimidos no pueden fraccionarse al tratarse de un citotóxico y deben manipularse con guantes. Si la presentación comercial no se ajusta a las necesidades del paciente deberá recurrirse a una fórmula magistral.
Los fármacos inmunomoduladores pueden tardar en hacer efecto y para observar una mejoría suele ser necesario que transcurran 3-4 semanas desde el inicio del tratamiento. Para conseguir un efecto más rápido cuando los signos clínicos son graves se pueden administrar conjuntamente glucocorticoides a dosis altas, con una pauta de disminución progresiva. Una vez conseguida la remisión, se puede continuar con el tratamiento de mantenimiento con el inmunomodulador. La combinación inicial de glucocorticoide e inmunomodulador permite conseguir un efecto rápido y continuado, ya que mientras se disminuye la dosis del glucocorticoide comienzan los efectos del inmunomodulador. La principal ventaja de los inmunomoduladores es que tienen menos efectos secundarios graves y su impacto general en la salud es menor.
Los glucocorticoides son los fármacos inmunosupresores empleados con más frecuencia. Inicialmente, se administran dosis altas para conseguir la remisión y después se disminuye la dosis gradualmente hasta la dosis mínima efectiva que consiga mantener la remisión y minimizar así los posibles efectos secundarios.
En muchas enfermedades autoinmunes es necesario instaurar un tratamiento adyuvante para disminuir la dosis de glucocorticoides y minimizar los efectos secundarios. En los casos más graves, puede ser necesario combinar varios inmunosupresores para conseguir y mantener la remisión de la enfermedad. Como muchos de estos fármacos pueden tener efectos secundarios hepáticos y en la médula ósea, es recomendable realizar un seguimiento cada 2-3 semanas durante el primer mes, y después cada 4-6 meses.
En caso de detectar cambios significativos en los parámetros sanguíneos hay que interrumpir la administración del fármaco y sustituirlo por otro. Los fármacos que se utilizan con más frecuencia en los tratamientos adyuvantes son la azatioprina, ciclosporina, micofenolato de mofetilo, ciclofosfamida y clorambucilo. Los perros más afectados pueden necesitar medidas de apoyo como el tratamiento de heridas abiertas, fluidoterapia y monitorización de las proteínas séricas. La inmunoglobulina intravenosa humana (IgIVh) ha demostrado buenos resultados en casos de dermatosis graves cuando otros tratamientos han fallado 6.
El tratamiento tópico puede ser de utilidad cuando las lesiones son localizadas o aparecen como brotes esporádicos. Los fármacos que se utilizan con mayor frecuencia en el tratamiento tópico son la betametasona y el tacrolimus. La betametasona ofrece la ventaja de controlar rápidamente la inflamación y los signos clínicos, pero a largo plazo puede provocar atrofia dérmica, por lo que si es necesario un tratamiento tópico de larga duración es preferible realizar una transición hacia el tacrolimus.
Tabla 1b. Fármacos frecuentes en el tratamiento de las dermatosis autoinmunes e inmunomediadas 1,24,25
El tratamiento de las dermatosis autoinmunes consta de 4 fases: fase de inducción, fase de transición, fase de mantenimiento y fase de curación 1. En la fase de inducción el objetivo es detener el componente inflamatorio de la enfermedad tan pronto como sea posible y suprimir la respuesta inmunológica dirigida contra la piel. Durante esta fase suele ser necesaria la administración de fármacos a dosis altas.
Si no se observa una respuesta adecuada, se debe considerar otro tipo de tratamiento; bien cambiando de fármaco o combinando el actual con uno nuevo. En la fase de transición las dosis se van reduciendo progresivamente con el objetivo de minimizar los efectos secundarios. Si se está utilizando una combinación de fármacos primero se debe reducir la dosis del fármaco con mayores efectos secundarios, como es el caso de los glucocorticoides. Las dosis se van disminuyendo lentamente, generalmente durante varias semanas o meses, hasta conseguir una dosis de mantenimiento aceptable o hasta que vuelvan a aparecer los signos clínicos. En este último caso, se aumenta la dosis hasta conseguir de nuevo la remisión de los signos y se vuelve a disminuir progresivamente hasta alcanzar la dosis mínima efectiva, que permita un control aceptable de los signos del paciente (fase de mantenimiento). En las dermatosis inmunomediadas se considera la “curación” cuando se ha conseguido la remisión de los signos, un control adecuado con el tratamiento de mantenimiento y, además, no se produce una recaída al suspenderlo.
La decisión de suspender el tratamiento de mantenimiento en un paciente bien controlado es complicada, especialmente, cuando la enfermedad era grave en su inicio. Esta decisión debe ser consensuada entre el veterinario y el propietario, por lo que es esencial asegurar la correcta información. El propietario debe ser consciente de que si se produce una recaída es más complicado volver a conseguir la remisión por segunda vez. La elección del momento en el que se puede interrumpir el tratamiento depende del tipo de enfermedad, de si se ha identificado y eliminado la causa desencadenante, y de los riesgos que conlleva para el paciente la suspensión del tratamiento. En muchos casos se recomienda que el tratamiento de mantenimiento se continúe al menos durante 8-12 meses antes de suspenderlo 1. Cuando los riesgos asociados a la recaída superan los beneficios de suspender el tratamiento, se debe mantener una terapia de por vida haciendo un seguimiento laboratorial adecuado.
No se recomienda vacunar a los pacientes con dermatosis autoinmunes, a pesar de que la causa desencadenante no sea la vacuna. Esta afirmación se basa en el hecho de que la vacunación puede estimular una respuesta inmune amplia e inespecífica, que posiblemente agrave la enfermedad autoinmune 7. La autora prefiere interrumpir la vacunación de la rabia y controlar los niveles de anticuerpos frente al parvovirus y moquillo. Si el título de anticuerpos no es suficiente como para mantener una inmunidad adecuada, se deben evaluar los riesgos y beneficios antes de revacunar al animal.
Tabla 1c. Fármacos frecuentes en el tratamiento de las dermatosis autoinmunes e inmunomediadas 1,24,25
Enfermedades específicas
Pénfigo foliáceo
El pénfigo foliáceo (PF) es la enfermedad autoinmune de la piel más frecuente en el perro, y cursa con una dermatitis que va de pustular a costrosa. El PF afecta a la epidermis, atacando a varias moléculas de adhesión, especialmente a los desmosomas, cuya función es mantener unidos a los queratinocitos. En el PF humano, los autoanticuerpos se dirigen principalmente frente a la glucoproteína desmogleína-1 (DSG1) del desmosoma 8, y aunque en el perro se ha sospechado esto mismo 9,10, actualmente, se cree que este autoantígeno es minoritario11 y hay evidencias que sugieren que el principal autoantígeno en el PF canino es la desmocolina-1 12.
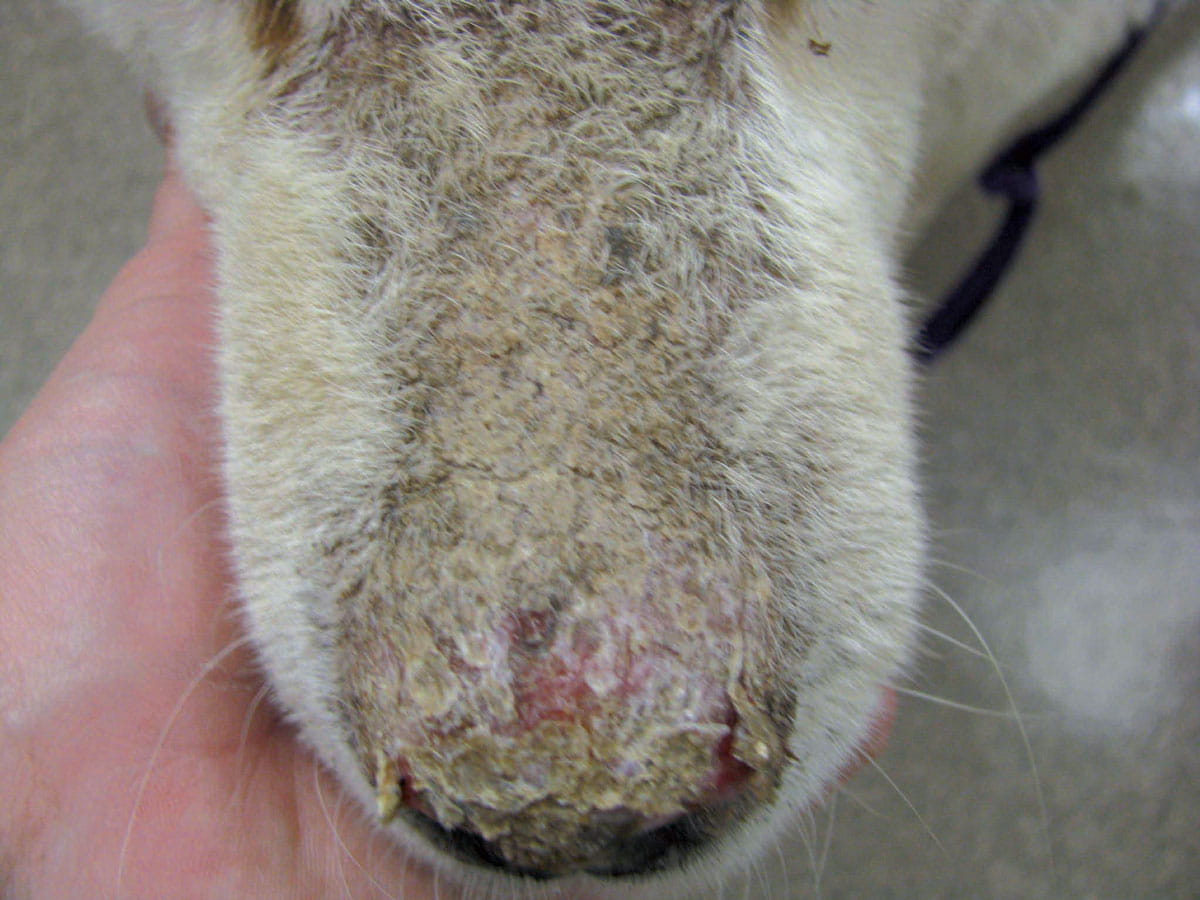
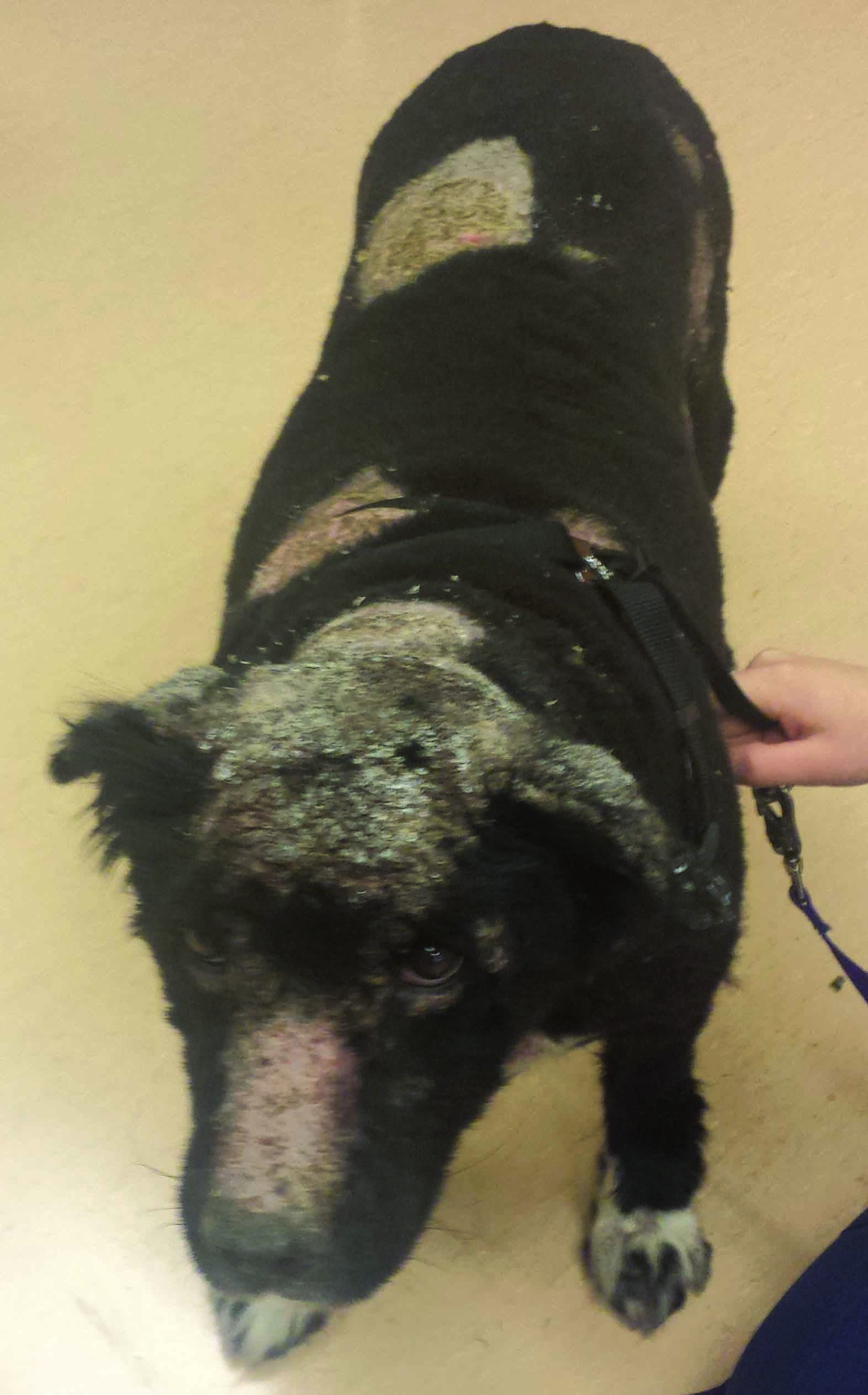
Los factores genéticos parecen desempeñar un papel importante en el desarrollo del PF. Se considera que las razas caninas con mayor riesgo de PF son el Akita y el Chow Chow 10. Entre los factores desencadenantes del proceso se incluyen las dermatosis alérgicas crónicas y los medicamentos (antibióticos, AINE, pipetas contra pulgas), pero el más importante es la luz ultravioleta 1,10. Las primeras lesiones que aparecen son las máculas, que progresan rápidamente hacia pústulas. Estas lesiones muchas veces son grandes y se fusionan. Las pústulas suelen ser frágiles, rompiéndose con facilidad y evolucionando hacia costras. Por tanto, el signo clínico más frecuente es la presencia de costras 1,9,10. Se pueden observar lesiones erosivas, y aunque las lesiones ulcerativas son muy poco frecuentes, pueden estar presentes en los casos complicados con una pioderma profunda. El PF se suele caracterizar por la presencia de costras inicialmente en la cara (especialmente en la zona dorsal del hocico, plano nasal, región periocular y pabellón auricular), y progresan extendiéndose de forma generalizada (Figura 2).
Con frecuencia, la citología de una pústula intacta o de la piel de debajo de la costra revela la presencia de numerosos neutrófilos no degenerados rodeando queratinocitos acantolíticos aislados o en grupo, cuya apariencia es la de queratinocitos de gran tamaño, nucleados, basófilos y redondos (Figura 1). En el estudio histopatológico se observan pústulas subcorneales con neutrófilos y un número variable de eosinófilos y queratinocitos acantolíticos 13. El tratamiento suele basarse en la administración de corticoesteroides a dosis altas con un inmunosupresor adyuvante, junto con el tratamiento tópico.
Figura 2. Pénfigo foliáceo: (a) Se pueden observar costras de color miel en la parte dorsal del hocico y en el plano nasal, donde hay además una ligera erosión producida al levantar la costra (b). Presentación más generalizada de pénfigo foliáceo.
© Amy Shumaker
Lupus eritematoso discoide
El lupus eritematoso discoide (LED), también conocido como lupus eritematoso cutáneo o “nariz de Collie”, es una enfermedad ulcerativa benigna que no tiene una implicación sistémica 1. Las lesiones generalmente se localizan en el plano nasal, aunque también pueden estar afectadas zonas del pabellón auricular expuestas al sol, región periocular y también se ha descrito una variante generalizada del LED 14. El signo clínico más frecuente es la pérdida inicial de la arquitectura adoquinada del plano nasal que progresa hacia la despigmentación y descamación (Figura 3). Al cronificarse la enfermedad pueden aparecer lesiones erosivas, ulcerativas y costrosas. En las variantes generalizadas se han observado placas hiperpigmentadas anulares o policíclicas en el cuello, tronco y extremidades. El estudio histopatológico revela una degeneración celular basal (apoptosis) con un infiltrado liquenoide pleocelular moderado en la dermis 13. Puesto que esta enfermedad puede asemejarse tanto clínica como histopatológicamente a la pioderma mucocutánea, puede ser útil realizar una citología del plano nasal de debajo de una costra. En caso de encontrar bacterias, se recomienda tratar la pioderma mucocutánea. En la mayoría de los casos de LED no es necesario utilizar un inmunosupresor potente, siendo eficaz para el control de la enfermedad el enfoque inmunomodulador con una tetraciclina (doxiciclina, minoclicina) y niacinamida, junto con el tratamiento tópico (esteroides tópicos, tacrolimus). En los casos más graves o refractarios puede ser necesario administrar inicialmente corticoesteroides a dosis altas. En las variantes generalizadas se ha documentado la eficacia de tratamientos con hidroxicloroquina o ciclosporina 14,15. Debido a que la luz solar tiene una influencia importante en el LED, es importante evitarla y utilizar protección solar para minimizar la exposición al sol. La suplementación con vitamina E (400 UI al día) puede ser beneficiosa.