Pathogénie
Plusieurs facteurs sont impliqués dans la pathogénie des dermatites à Malassezia, tels que les mécanismes d’adhésion aux cellules cornées de l’hôte, les interactions avec les autres organismes symbiotiques, ainsi que la réponse immunitaire de l’hôte.
L’adhésion aux cornéocytes du chien pourrait jouer un rôle important dans la pathogénie des dermatites à Malassezia chez certains individus. Les parois cellulaires des levures, composées de chitine, glucane, chitosane et mannane 1, contiennent des protéines ou glycoprotéines sensibles à la trypsine qui contribuent à l’adhésion aux cornéocytes canins. M. pachydermatis exprime également spécifiquement des adhésines qui se lient aux résidus glucidiques mannosylés à la surface des cornéocytes du chien. Toutefois, ce mécanisme d’adhésion n’intervient apparemment pas dans la pathogénie des dermatites à Malassezia chez le Basset Hound (race prédisposée à la prolifération des Malassezia) mais il semble important dans d’autres races 10.
M. pachydermatis a visiblement une relation symbiotique avec les espèces commensales de staphylocoques, mais l’hypothèse selon laquelle les dermatites à Malassezia seraient induites par les antibiotiques n’a pas été confirmée. Ces deux micro-organismes produisent des facteurs de croissance et des modifications micro-environnementales qui leur sont mutuellement bénéfiques ; le nombre de Staphylococcus pseudintermedius ou de S. intermedius est donc plus élevé chez les chiens porteurs de Malassezia 1,4,8. En effet, 40 % des chiens souffrant d’une prolifération de Malassezia souffrent également d’une pyodermite à staphylocoques 3,11.
La levure peut déclencher une réaction immunitaire chez l’hôte. L’immunité humorale est stimulée, comme en témoigne l’élévation du taux d’anticorps dirigés contre les antigènes des levures chez les chiens présentant une dermatite à Malassezia par rapport aux chiens sains 12,13. Toutefois, les taux élevés d’IgA et d’IgG présents chez les chiens souffrant de dermatite à Malassezia ne semblent procurer aucune protection supplémentaire contre cette infection fongique. L’immunité à médiation cellulaire pourrait jouer un rôle plus important dans la protection contre la maladie. Par exemple, le Basset Hound semble avoir une réponse lymphocytaire vis-à-vis des Malassezia diminuée par rapport aux chiens sains chez lesquels la levure ne prolifère pas 14.
Un phénomène d’hypersensibilité, dû aux produits sécrétés par la levure et à ses antigènes de surface, pourrait également intervenir 4,8. En adhérant aux cornéocytes canines, la levure sécrète différentes substances incluant le zymosane et différentes enzymes – uréase, protéases, phosphohydrolase, phospholipases (notamment phospholipase A2), lipoxygénases, phosphatases, glucosidase, galactosidase, et leucine arylamidase. Ces facteurs de virulence induisent une modification du pH local, une protéolyse, une lipolyse, une activation du complément, et une libération locale d’éicosanoïdes, provoquant inflammation et prurit 1,4,8. En outre, des taux supérieurs d’IgE spécifiques dirigés contre des allergènes de Malassezia de poids moléculaires 45, 52, 56 et 65 kDa ont été mis en évidence chez des chiens atopiques par rapport aux témoins sains, ce qui renforce encore l’hypothèse d’une hypersensibilité à la levure 15.
Facteurs prédisposant à la pathogénicité
Plusieurs facteurs peuvent favoriser le passage de l’état commensal à l’état pathogène : prédisposition génétique (déplacement), dysfonctionnement immunitaire, humidité accrue, intertrigo, dysendocrinies, troubles de la kératinisation, hypersensibilités, et prolifération bactérienne de surface concomitante.
L’humidité pourrait jouer un rôle important car les Malassezia semblent être plus nombreuses dans les sites corporels humides comme les conduits auditifs et les plis de peau, et leur prévalence augmente dans les climats humides 1. Les dysendocrinies, telles que l’hypothyroïdie, l’hypercorticisme spontané et iatrogène, et le diabète sucré pourraient augmenter la disponibilité des nutriments et des facteurs de croissance nécessaires à la levure. Cela pourrait être dû à une modification des concentrations cutanées en acides gras, une anomalie de la lipogénèse kératinocytaire et un dysfonctionnement des glandes sébacées 16,17. Les races Cocker Américain, Shih Tzu, Setter Anglais, West Highland White Terrier, Basset Hound, Caniche Nain et Toy, Boxer, Terrier Australien, Silky Terrier, Cavalier King Charles, Teckel, et Berger Allemand semblent être prédisposées à la dermatite à Malassezia, ce qui suggère l’existence d’une composante génétique 4,6,8. Un dysfonctionnement des IgA sécrétoires ou de l’immunité à médiation cellulaire pourrait également contribuer à la pathogénicité chez certains chiens 2,4. Par exemple, une baisse in vitro de l’activité blastogène des lymphocytes en réponse aux antigènes de M. pachydermatis a été observée chez des Bassets Hound atteints de dermatite à Malassezia par rapport à des Bassets Hound sains 14. Les hypersensibilités, de type dermatite allergique aux piqûres de puces, réaction cutanée d’origine alimentaire, et dermatite atopique, pourraient également prédisposer les chiens aux dermatites à Malassezia par induction de la cascade inflammatoire et d’un prurit consécutif.
En résumé, toutes les dermatoses entraînant une perte d’intégrité de la couche cornée, qu’elle soit mécanique (due à un prurit) ou biochimique (due à une dysendocrinie, des troubles de la kératinisation ou de l’immunité), peuvent potentiellement permettre aux facteurs de virulence des Malassezia de rencontrer le système immunitaire sous-corné, et donc à la levure de devenir pathogène.
Diagnostic
Tableau clinique
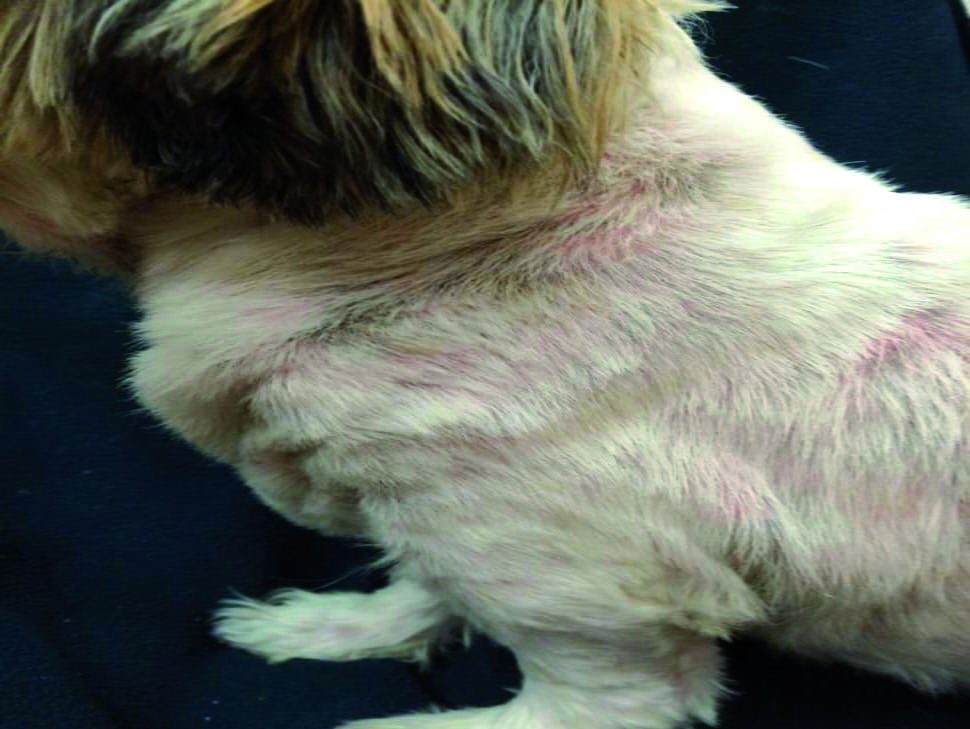
Les lésions cutanées de la dermatite à Malassezia peuvent être localisées (Figure 2) ou généralisées. Elles se développent habituellement dans les zones chaudes et humides telles que les plis de peau, les conduits auditifs, l’aine, la face ventrale du cou, la face médiale des cuisses, les espaces interdigités, les régions périanale et périvulvaire, et les autres zones intertrigineuses (Figure 3). Des dermatoses concomitantes, de type pyodermite staphylococcique, allergies cutanées ou troubles de la kératinisation, sont présentes chez 70 % des chiens touchés 1,4. Les lésions apparaissent généralement pendant les mois humides d’été – correspondant aussi aux pics d’allergies saisonnières – et peuvent persister jusqu’à la fin de l’hiver. Les animaux ne répondent pas à la corticothérapie.