Internados de veterinaria en Estados Unidos
¿Estás pensando en hacer un internado en Estados Unidos? Este artículo resume brevemente las posibles ventajas y desventajas de estos programas de formación.
Número de edición 32.3 Otros artículos científicos
Fecha de publicación 12/04/2023
Disponible también en Français , Deutsch , Italiano y English
La sepsis en el perro es una urgencia veterinaria y es esencial su rápida identificación y la intervención proactiva para que el pronóstico sea favorable.

La presencia de sepsis se debe considerar una urgencia médica y su diagnóstico rápido es esencial para el pronóstico favorable.
La transición de sepsis a disfunción orgánica múltiple y shock séptico se puede prevenir con una reanimación rápida y adecuada.
La antibioterapia es esencial en los pacientes críticos con sospecha de sepsis y signos de shock.
Hay que evaluar y revaluar continuamente al paciente: la sepsis evoluciona constantemente y requiere un estrecho seguimiento de la respuesta al tratamiento.
La sepsis es una urgencia médica que se conoce desde los tiempos de Hipócrates, en torno al 400 a. C., cuando se asoció a cualquier afección que producía la putrefacción de la carne. Unos 1.400 años más tarde, el médico persa Avicena describió la sepsis como la putrefacción de la sangre y de los tejidos con presencia de fiebre 1. Hoy en día sabemos que este proceso provoca una enfermedad sistémica debida a la respuesta descontrolada del sistema inmune a la infección. Esto puede conducir a la disfunción de uno o más órganos, que es la causa de mortalidad más frecuente en pacientes con sepsis, por lo que es sumamente importante que el diagnóstico y el tratamiento se realicen de forma precoz.
Las primeras definiciones de sepsis en la medicina moderna se establecieron en 1991 (denominadas Sepsis - 1), y aunque se han modificado con el transcurso de los años (Sepsis - 2 y - 3), los conceptos iniciales siguen siendo los que más se utilizan a efectos prácticos en medicina veterinaria 2. La idea inicial fue la de unificar criterios y establecer las pautas que pudiesen ayudar a reconocer y tratar al paciente con sepsis de la manera más rápida y eficaz posible. Estos conceptos incluyen:
Tabla 1. Criterios para la identificación de un perro con SIRS.
| Temperatura (°C/F) | ≤ 37,2/99,0 o ≥ 39,2/102,5 |
| Frecuencia cardiaca (latidos/min) | ≥ 140 |
| Frecuencia respiratoria (respiraciones /min) | > 20 |
| Leucocitos (x 103/µL) | ≥ 16 o ≤ 6 |
| En banda (%) | ≥ 3 |
La clave radica en comprender el concepto de SIRS. El SIRS es la respuesta sistémica a cualquier alteración que causa inflamación, ya sea a nivel global, como en el paciente tras un golpe de calor, o local, como en la pancreatitis aguda. El organismo es incapaz de mantener la respuesta inflamatoria exclusivamente en el foco original, por lo que el proceso inflamatorio comienza a afectar a tejidos normales de otras áreas del cuerpo no relacionadas con la causa original, extendiéndose de forma generalizada. Por lo tanto, independientemente de la causa inicial, todos los sistemas corporales pueden mostrar signos de inflamación. Si el origen del proceso inicial es infeccioso, el paciente es séptico por definición; en otras palabras, todos los pacientes sépticos presentan SIRS, pero no todos los pacientes con SIRS tienen sepsis (p. ej., traumatismos, golpe de calor, pancreatitis).
Tabla 2. Definiciones de disfunción orgánica en el perro.
| Sistema | Criterio |
|---|---|
| Renal |
Diuresis < 0,5 ml/kg/h en ≥ 12 horas o aumento de la creatinina sérica ≥ 0,3 mg/dl sin evidencia de azotemia pre- o post-renal
|
| Cardiovascular |
Hipotensión que requiere el uso de vasopresores
|
| Respiratorio |
Es necesaria la administración de oxígeno o la ventilación asistida, según la exploración física, la gasometría arterial (gradiente arterial– alveolar > 10 mmHg y/o pulsioximetría (SpO2 < 95%)
|
| Hígado |
Bilirrubina total en suero o plasma > 0,5 mg/dl
|
| Coagulación |
Tiempo de protrombina o tiempo de tromboplastina parcial activada > 25% del límite superior de referencia y/o recuento de plaquetas 100 000/µL
|
Basándonos en los conceptos anteriores, el primer paso consiste en determinar si un paciente presenta una respuesta inflamatoria sistémica. Para ello, se utilizan unos criterios que incluyen alteraciones en la frecuencia respiratoria (taquipnea), la frecuencia cardiaca (bradicardia o taquicardia) y la temperatura rectal (hipotermia o fiebre), así como en el leucograma (leucopenia o leucocitosis con o sin desviación a la izquierda) (Tabla 1). La presencia de dos o más de estos criterios en un perro es suficiente para confirmar SRIS 3. El valor diagnóstico de estos criterios radica en su sencillez al no ser necesarias pruebas más sofisticadas y permitir identificar rápidamente al paciente. El mayor problema es que estos criterios no son específicos y la gran mayoría de los pacientes ingresados cumplen con uno o varios criterios de SIRS. Como regla general, cuantos más criterios cumpla un paciente, mayor es la probabilidad de SIRS. Un perro con taquicardia, taquipnea, fiebre y leucocitosis tiene muchas más probabilidades de presentar SIRS que uno con taquicardia y taquipnea en el que, por ejemplo, el estrés y la ansiedad de estar en la clínica podrían provocar estas alteraciones.
El siguiente paso consiste en determinar si el origen del proceso inflamatorio sistémico es infeccioso (es decir, si el paciente tiene sepsis) o no. Para ello, primero se deben tener en cuenta los datos de la historia clínica y de la exploración física (Figura 1). En algunos casos, la causa inicial se puede establecer fácilmente, como cuando se observa un absceso cutáneo tras una mordedura. En otros casos, esto puede resultar más complicado, siendo necesaria una investigación más exhaustiva. Siempre que se sospeche sepsis es recomendable realizar, como mínimo, un análisis de sangre completo (hemograma y bioquímica) y un análisis de orina (con cultivo). En los resultados de los análisis de sangre se puede observar, por ejemplo, leucocitosis o leucopenia, trombocitopenia, hipoalbuminemia, hiperbilirrubinemia, hipocalcemia, azotemia e hiper- o hipoglucemia, que son las alteraciones más frecuentes en los pacientes con sepsis. Estos análisis iniciales se pueden complementar con otras pruebas diagnósticas para buscar el foco infeccioso, incluyendo las radiografías de tórax, abdomen y/o columna vertebral (Figura 2), así como la ecografía abdominal y/o torácica y otras pruebas de imagen que estén disponibles (Figura 3), el análisis del líquido cefalorraquídeo y/o de la punción articular, la serología y/o prueba de PCR para enfermedades infecciosas en función de la presentación clínica y la localización geográfica. Como norma general, cualquier acumulación anormal de líquido se debe examinar mediante citología, ya que la presencia de bacterias intracelulares confirmará la infección, y se debe conservar una muestra para el posterior cultivo y antibiograma en caso necesario (Figura 4). Si se sospecha una peritonitis séptica en un paciente, pero no se encuentran bacterias intracelulares en el líquido peritoneal, se puede realizar la comparación entre la concentración de glucosa en sangre y la concentración de glucosa en el líquido peritoneal; una diferencia superior a 20 mg/dl (sangre > líquido peritoneal) es compatible con el diagnóstico de peritonitis séptica 4. Sin embargo, aunque en un paciente se sospeche inicialmente la presencia de infección, no siempre será posible confirmarlo, por lo que el veterinario debe considerar otras posibilidades o monitorizar la respuesta al tratamiento, revaluando frecuentemente al paciente.

Figura 1. Mucosa oral congestiva en un perro con SIRS.
© Rocío Redondo

Figura 2. Radiografía torácica lateral de un perro con neumonía por aspiración. Obsérvese la presencia de broncograma aéreo en los lóbulos pulmonares craneales, derecho e izquierdo, y en el medial derecho; además existe una dilatación esofágica generalizada.
© Rafael Obrador de Aguilar
La presentación clínica del perro con sepsis puede ser muy variable y mientras algunos pacientes necesitan un tratamiento intensivo para sobrevivir, otros pueden recibir el tratamiento de forma ambulatoria. Los aspectos importantes para la estabilización de estos pacientes son la reanimación, el control de la fuente de infección, la antibioterapia y la utilización de vasopresores (en caso de shock séptico).
 |
| a |
 |
| b |
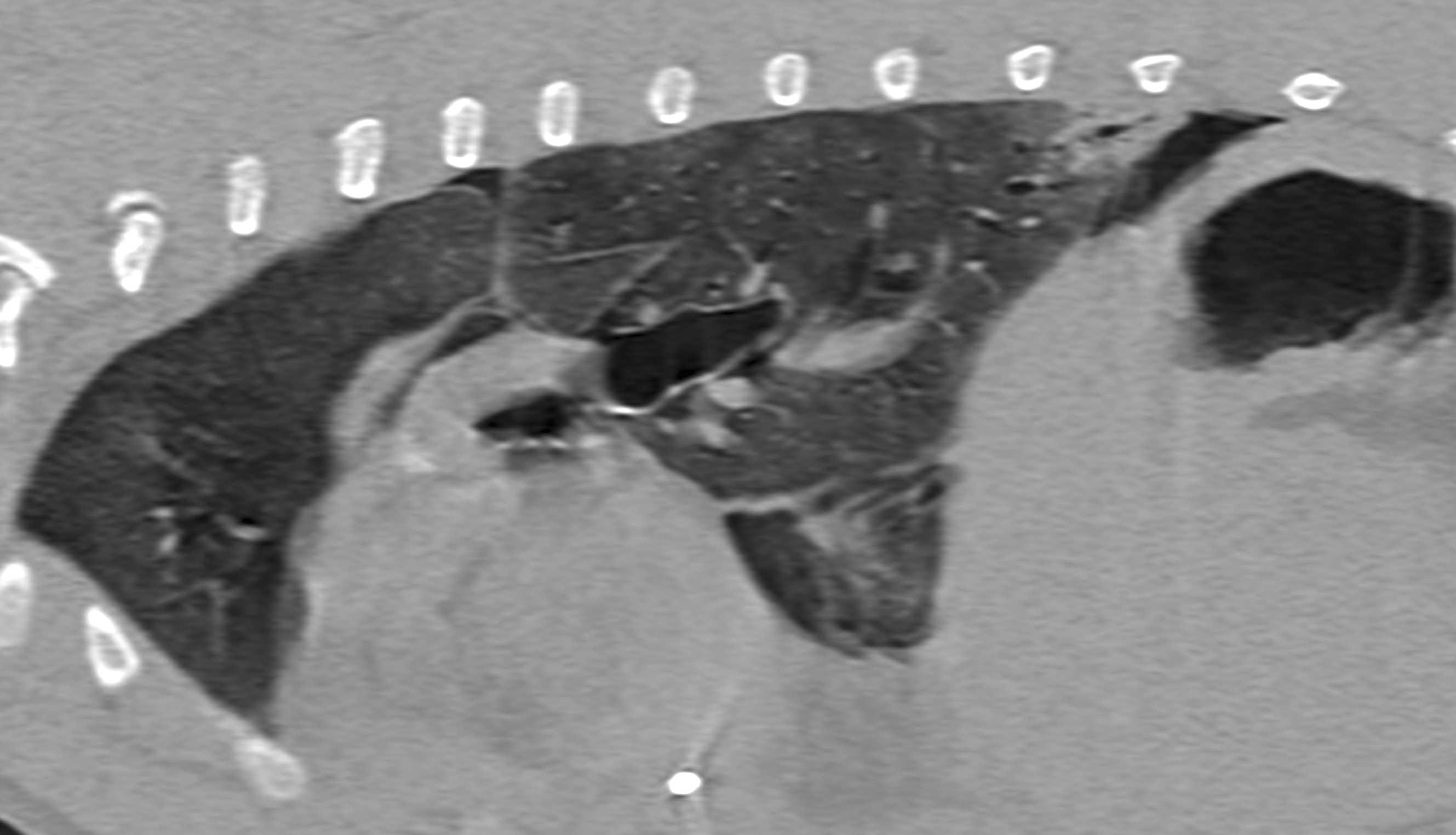
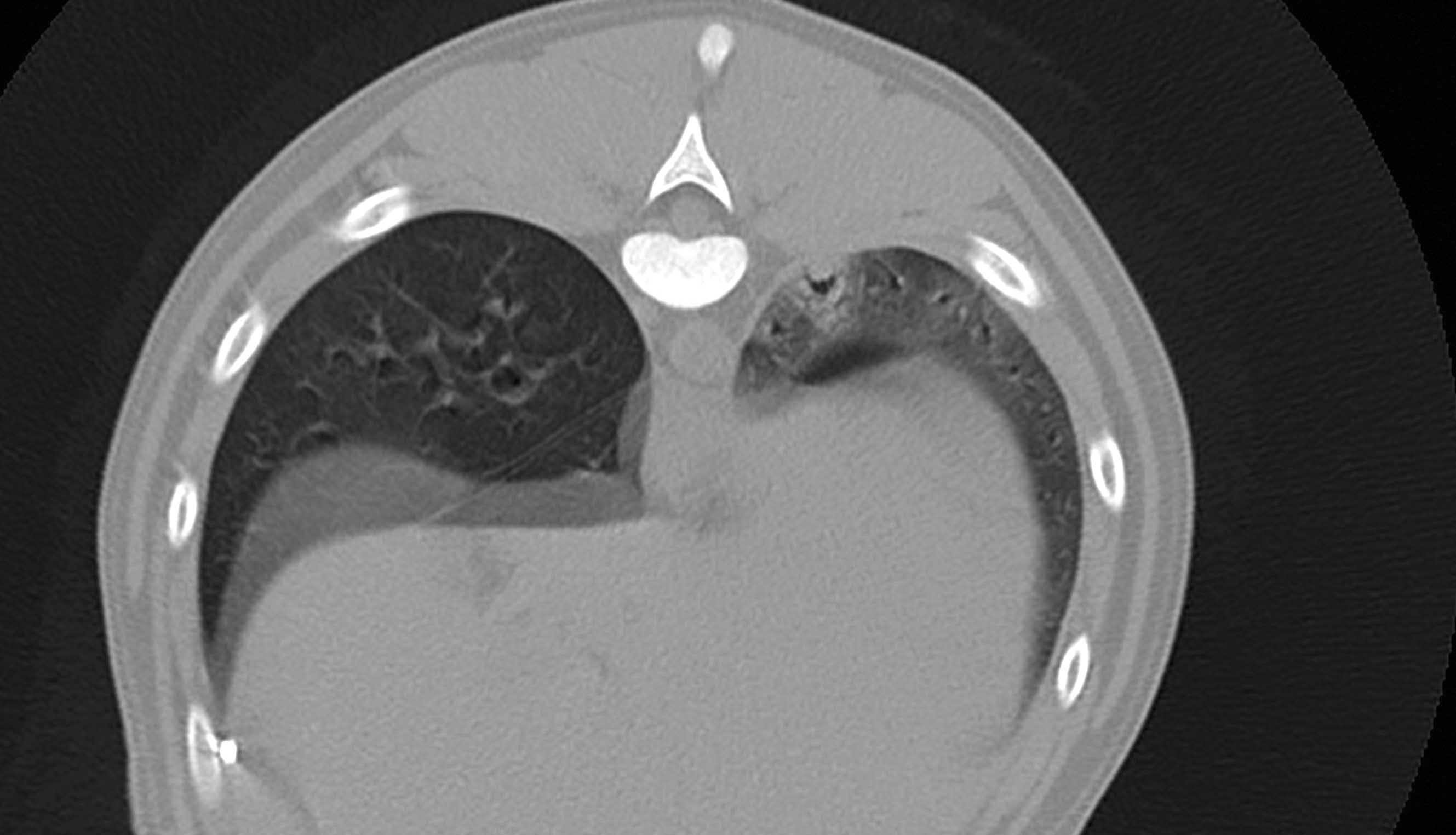
Figura 3. Imagen sagital (a) y transversal (b) obtenida por tomografía computarizada en un paciente con sepsis y piotórax secundario a la migración de una espiga. El lóbulo pulmonar caudal izquierdo se encuentra más alejado de la pared torácica y muestra un patrón alveolar focal; también se observa un pequeño broncograma aéreo.
© Rafael Obrador de Aguilar
La reanimación del perro con sepsis es diferente a la del paciente con otras formas de shock. En la sepsis, la causa del fallo hemodinámico es la combinación de hipovolemia absoluta (siendo beneficiosa la administración de fluidos) e hipovolemia relativa como consecuencia del aumento de la permeabilidad vascular, lo que provoca la pérdida de fluidos, la pérdida del tono vascular y, en algunos casos, la disfunción miocárdica. El grado en el que cada uno de estos factores puede afectar a un paciente determinado es muy variable y dinámico. Es lógico suponer que una misma estrategia terapéutica no beneficiará a todos los pacientes por igual, por lo que es mucho mejor individualizar el protocolo de fluidoterapia en función de las necesidades de cada animal.
 |
 |
| a | b |
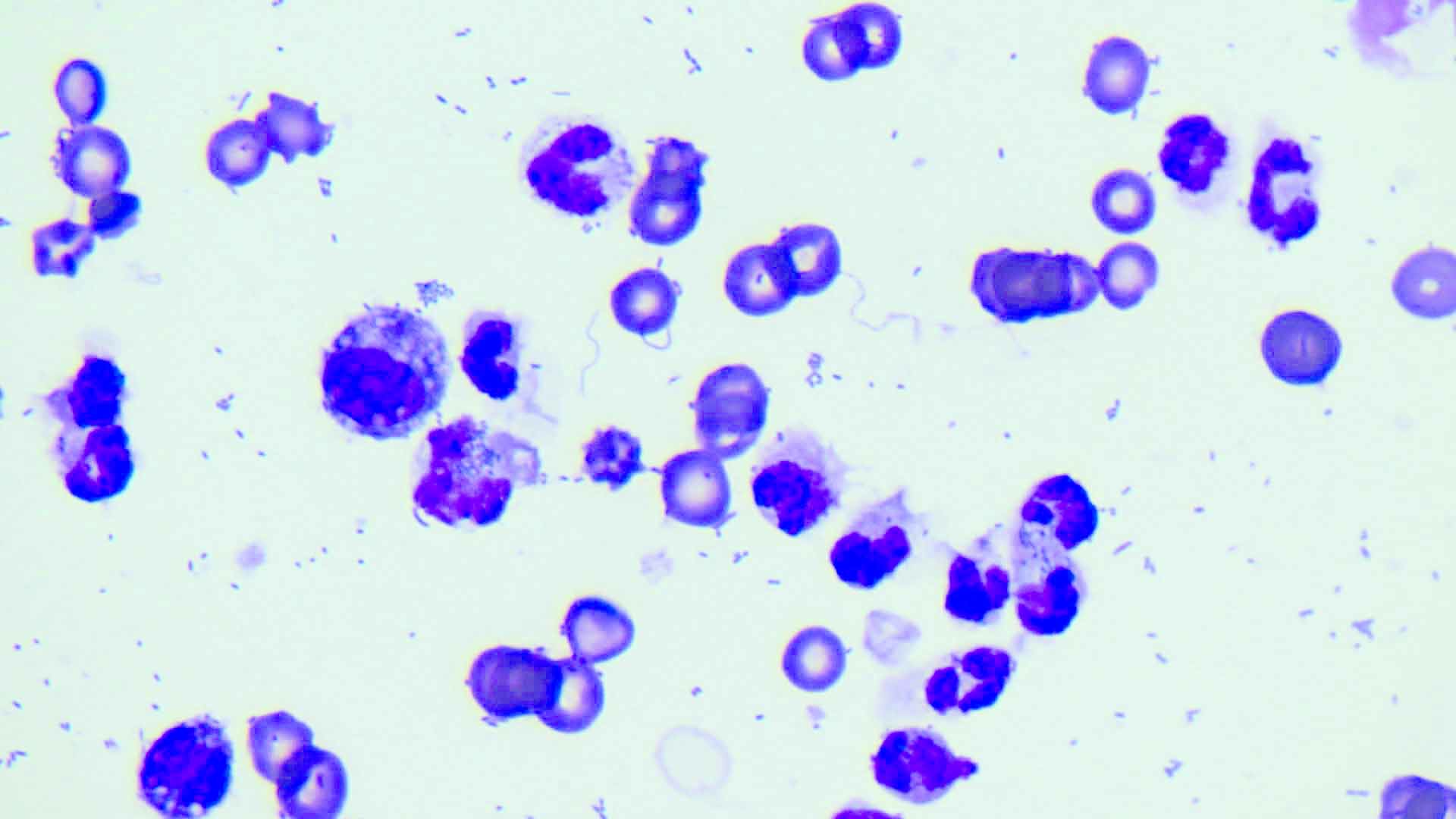
Figura 4. (a) Muestra obtenida por abdominocentesis en un paciente con abdomen séptico. (b) La citología del líquido evidencia la presencia de bacterias intracelulares (aumento x100).
© Rafael Obrador de Aguilar
Actualmente, aunque no se ha demostrado que una estrategia de administración de fluidos (tipo, volumen y frecuencia) sea superior a otra para la reanimación del paciente con sepsis, lo que sí que es muy importante es la rapidez de la reanimación una vez detectadas las alteraciones hemodinámicas; lo ideal es que se realice en unos 20-30 minutos siempre que sea posible. De hecho, la administración precoz de fluidos puede modular el proceso inflamatorio e incluso disminuir la necesidad de utilizar vasopresores (Figura 5). Sin embargo, la administración tardía o inadecuada de fluidos está asociada con el agravamiento del estado hemodinámico, del flujo sanguíneo de la microcirculación y de la disfunción orgánica 5,6,7. Por lo tanto, se recomienda iniciar la reanimación con un cristaloide isotónico equilibrado (p. ej., Ringer Lactato) 8. Normalmente se administra un bolo intravenoso (10-20 ml/kg en unos 15 minutos) mientras se monitorizan los parámetros de perfusión (estado mental, frecuencia cardiaca, color de las mucosas, tiempo de relleno capilar, temperatura de las extremidades, calidad del pulso) con el objetivo de mejorar o incluso restablecer estos parámetros a la normalidad. Si la respuesta del paciente no es favorable (es decir, los parámetros de perfusión no mejoran adecuadamente), el bolo se puede repetir dos o tres veces, comprobando que no haya signos de una posible sobrecarga de volumen (temblores, náuseas, jadeo, quemosis, secreción nasal serosa, aumento de la frecuencia y/o esfuerzo respiratorio, edema subcutáneo, crepitaciones en la auscultación pulmonar); si esto ocurre, la administración de más fluidos será perjudicial y no está indicada.
Una vez reanimado el paciente, el plan de fluidoterapia se debe ajustar, como con cualquier paciente hospitalizado, en función de la deshidratación, las necesidades fisiológicas diarias y las posibles pérdidas continuas de líquido. Sin embargo, alrededor del 15% de los pacientes con sepsis evolucionan a shock séptico, caracterizado por fallo circulatorio, disfunción orgánica múltiple y aumento de la mortalidad. En este punto, ni siquiera la administración adecuada de fluidos consigue revertir la hipotensión sistémica debida al proceso séptico y es necesario utilizar vasopresores (ver a continuación).

Figura 5. La administración de fluidos en el perro con shock séptico debe iniciarse tan pronto como sea posible, utilizando un cristaloide isotónico equilibrado.
© Shutterstock
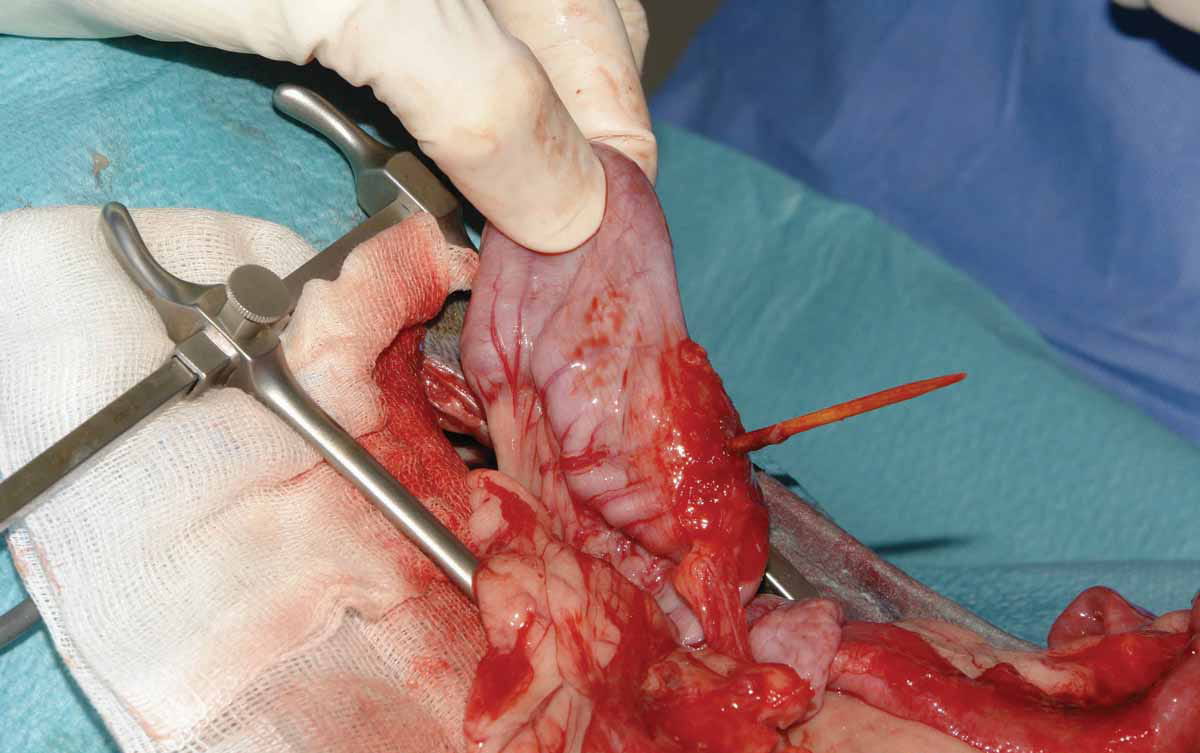
El control del foco infeccioso permite eliminar la causa original y evitar la posible progresión a disfunción orgánica en pacientes con sepsis. Por lo tanto, una vez conseguida la reanimación, es fundamental drenar o eliminar quirúrgicamente el tejido infectado lo antes posible, ya que se ha demostrado que la eliminación adecuada y temprana del foco infeccioso influye positivamente en el pronóstico del paciente (Figura 6) 9. Además, este procedimiento también permite obtener muestras microbiológicas para su análisis.
 |
| a |
 |
| b |
 |
| c |
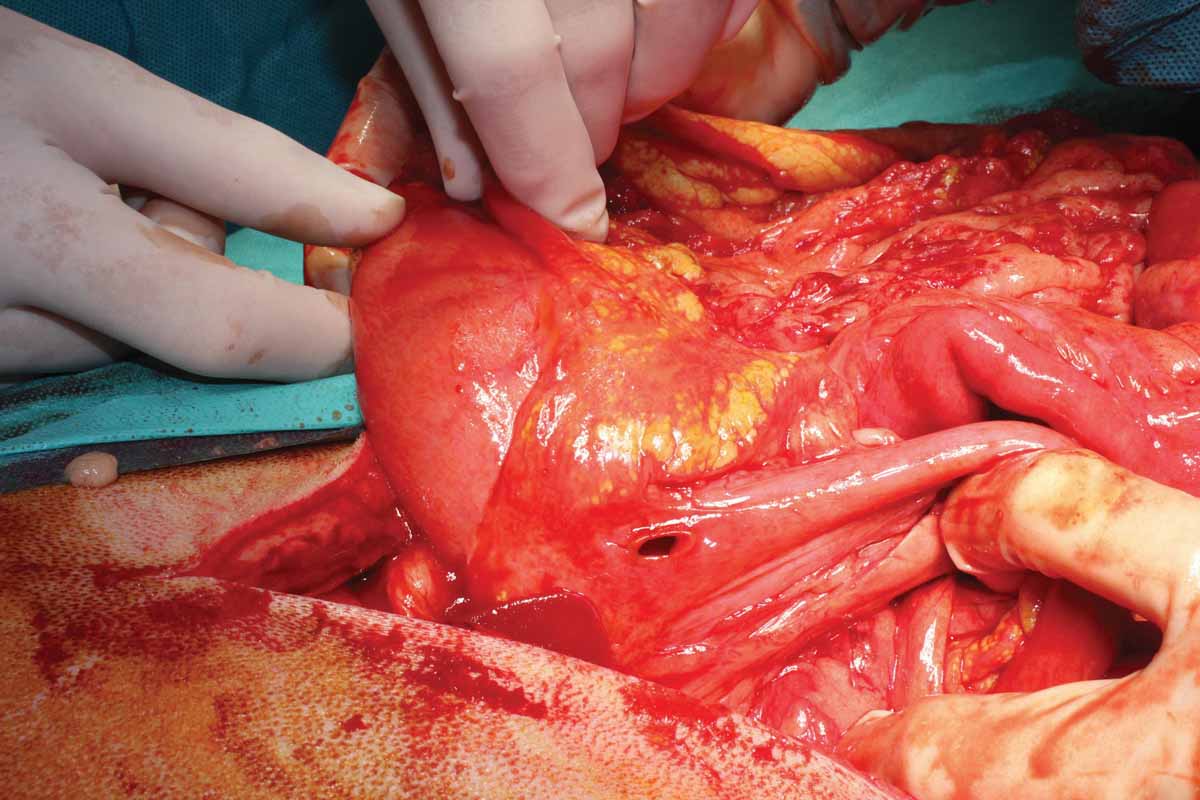
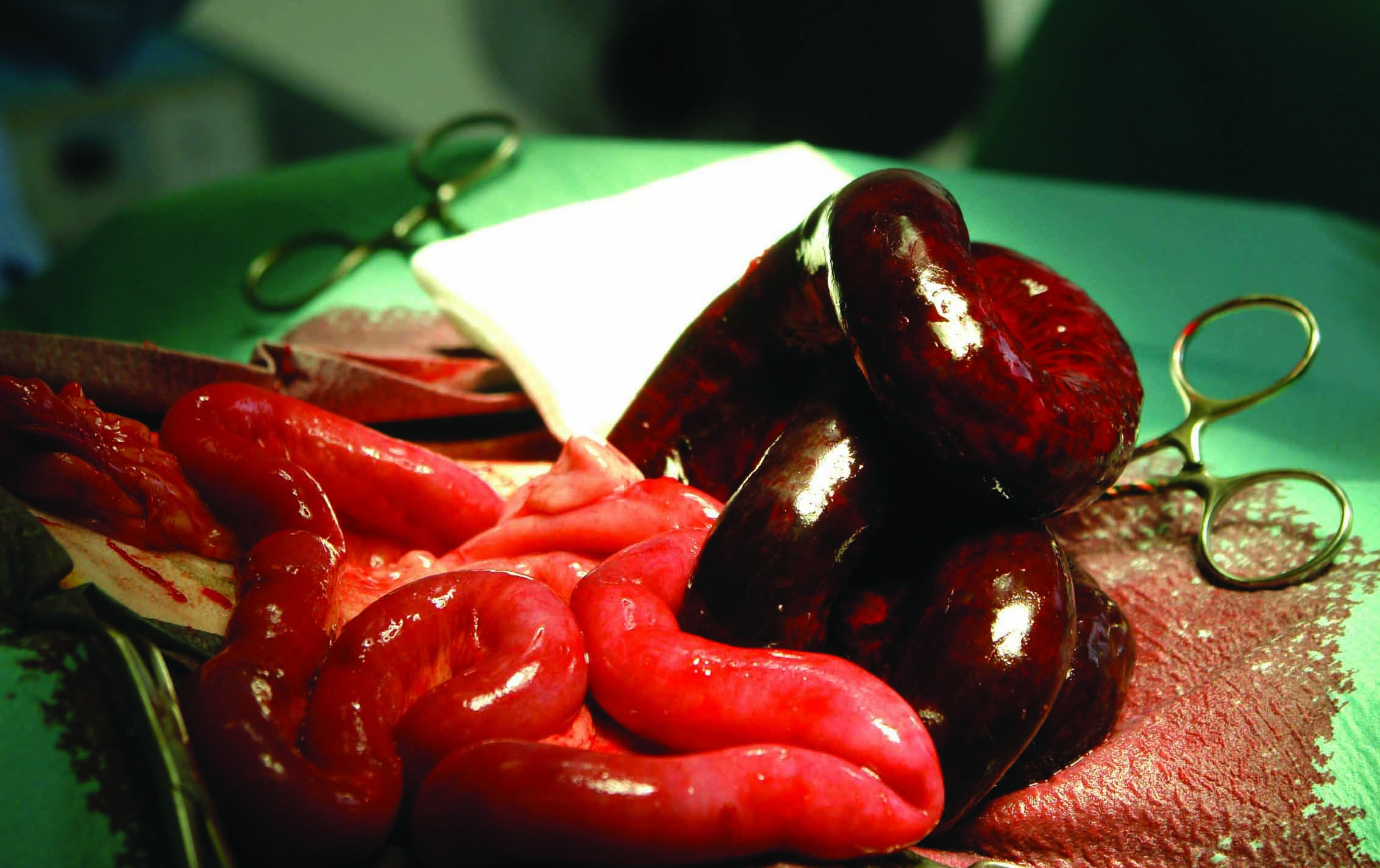
Figura 6. Ejemplos de abdomen séptico: (a) perforación duodenal secundaria a fármacos antiinflamatorios no esteroideos; (b) perforación intestinal por un cuerpo extraño; y (c) torsión mesentérica.
© Nuria Vizcaíno
La administración temprana de la antibioterapia adecuada es uno de los pilares fundamentales del tratamiento de la sepsis, especialmente en los pacientes más críticos, como los que presentan disfunción orgánica o shock séptico. Siempre que sea posible, y no retrase la administración de antibióticos, es recomendable obtener las muestras para el cultivo y el antibiograma. El tratamiento empírico es necesario al principio, hasta obtener los resultados del análisis de las muestras, seleccionando un antimicrobiano de amplio espectro que probablemente sea eficaz contra los microorganismos potencialmente responsables del problema. Otros factores que deben tenerse en cuenta son el estado del paciente (si el antibiótico de elección requiere administración oral o intravenosa) y la posibilidad de infecciones multirresistentes (por exposición previa a antibióticos, hospitalizaciones recientes o infección adquirida en el hospital). La dosis debe ser la adecuada para maximizar la erradicación del patógeno, minimizando al mismo tiempo la posibilidad de desarrollar resistencias antimicrobianas y evitando reacciones adversas. Algunos ejemplos de combinaciones de antibióticos para pacientes con sepsis que requieren ser hospitalizados y no han recibido antibióticos en las semanas previas al ingreso incluyen 10:
La combinación empírica elegida se debe ajustar posteriormente en función de la evolución del paciente y de los resultados del cultivo/antibiograma. Esto es la denominada desescalada, cuyo objetivo es ajustar el espectro y el número de antibióticos al mínimo imprescindible para lograr el control adecuado del cuadro infeccioso una vez identificado el microorganismo. Esta práctica demuestra un uso racional de los antibióticos, al minimizar los posibles efectos secundarios y ayudar a evitar la aparición de resistencias bacterianas.
Si en el paciente séptico se detecta hipotensión sistémica (presión arterial sistólica < 90 mmHg) y no está respondiendo a la reanimación con fluidos (shock séptico), el tratamiento con vasopresores se debe iniciar cuanto antes 11. La administración precoz de vasopresores en pacientes con shock séptico se ha asociado con un menor volumen de fluidos de reanimación, una menor acumulación tisular de fluidos y una menor duración de la hipotensión, lo que podría reducir la mortalidad en estos pacientes 12. El objetivo es intentar aumentar la resistencia vascular sistémica al mejorar la presión arterial y mantener así la perfusión de los órganos vitales. La presión sistólica se debe mantener por encima de 90-100 mmHg si previamente la presión arterial del paciente era normal.
Los dos fármacos vasopresores utilizados con más frecuencia en medicina veterinaria son la noradrenalina (norepinefrina) y la dopamina (Tabla 3). La noradrenalina es una catecolamina que aumenta la presión arterial, principalmente debido a sus propiedades vasoconstrictoras, con un efecto mínimo sobre la frecuencia cardiaca (efecto α-1 marcado y efecto β-1 moderado). Además, con la reanimación adecuada de volumen, la noradrenalina mejora el flujo sanguíneo renal y disminuye los niveles de lactato. La dopamina es el precursor natural de la noradrenalina en el organismo, aunque sus efectos son ligeramente diferentes y dependientes de la dosis utilizada. En general y en comparación con la noradrenalina, sus efectos a dosis intermedias (3-10 µg/kg/min) son más marcados a nivel cardiaco (β-1) y más débiles a nivel vascular (α-1), existiendo un mayor riesgo de taquicardia y/o arritmias, por lo que este fármaco se utiliza con menos frecuencia que la noradrenalina. Sin embargo, la elección depende en última instancia de la preferencia personal del veterinario y lo familiarizado que esté con el uso de uno u otro.
Tabla 3. Vasopresores utilizados en el perro: mecanismo de acción y dosis recomendadas.
| Vasopresor | α | β1 | β2 |
Contractibilidad | Frecuencia cardiaca | Tono vascular | Presión arterial | Dosis |
|---|---|---|---|---|---|---|---|---|
| Dobutamina | + | + | ++ | ↑↑ | ↑ | ↓ | Variable | 5-20 µg/kg/mi |
| Dopamina | ++ | + | ++ | ↑↑ | ↑↑ | ↑↑ | ↑↑ | 5-20 µg/kg/min |
| Adrenalina | +++ | +++ | +++ | ↑↑↑ | ↑↑↑ | ↑↑↑ | ↑↑↑ | 0,05-1,0 µg/kg/min |
| Noradrenalina | +++ | + | 0 | ↑ | Variable | ↑↑↑ | ↑↑↑ | 0,1-2,0 µg/kg/min |
| Vasopresina | 0 | 0 | 0 | 0 | ↓ | ↑↑ | ↑↑ |
0,5-5,0 mU/kg/min
|
Ambos fármacos se administran en infusión continua intravenosa, utilizando inicialmente una dosis del intervalo inferior recomendado para aumentarla gradualmente hasta conseguir estabilizar hemodinámicamente al paciente (presión sistólica > 90-100 mmHg). Sin embargo, en algunos perros con shock séptico, la hipotensión puede no mejorar a pesar de la administración de fluidos y de dosis altas de vasopresores, situación que se denomina shock refractario 13. En estos casos, se debe volver a evaluar al paciente e investigar las posibles causas de shock refractario (Tabla 4).
Tabla 4. Causas de shock refractario.
|
Los glucocorticoides no están recomendados en pacientes con sepsis cuando la reanimación con fluidoterapia y/o vasopresores permite mantener la estabilidad hemodinámica. Sin embargo, si un perro con shock séptico no ha respondido a la expansión de volumen y sigue presentando hipotensión, a pesar de la administración de altas dosis de catecolaminas, el uso de corticosteroides se debe considerar 14,15. Estos fármacos aumentan la respuesta vascular α-adrenérgica y disminuyen la vasodilatación derivada de la inflamación. Las pautas recomendadas incluyen la administración de hidrocortisona en bolo intravenoso (1 mg/kg) seguido de 0,08 mg/kg/h en infusión continua 16) o la administración de dexametasona en infusión continua (0,01-0,02 mg/kg/h).
El tracto digestivo se considera el “órgano de shock” en la especie canina y, por tanto, es susceptible de sufrir problemas de hipoperfusión, ya que el flujo sanguíneo se desvía hacia los órganos más importantes en caso de necesidad. Este efecto, junto con la presencia de anorexia, puede afectar significativamente a la permeabilidad de la barrera gastrointestinal, con la posibilidad de translocación bacteriana (y de endotoxinas). Además, los pacientes sépticos con anorexia son particularmente susceptibles a la desnutrición, de ahí la importancia de iniciar la nutrición lo antes posible, pero primero, el paciente debe estar hidratado y hemodinámicamente estable, sin presentar alteraciones electrolíticas significativas. La nutrición enteral puede ser voluntaria o mediante sondas de alimentación en pacientes sin interés por el alimento. El objetivo inicial es aportar nutrientes a los enterocitos para mantener la función de barrera gastrointestinal, por lo que inicialmente pueden no alcanzarse las necesidades energéticas en reposo (NER) del perro, calculadas según la fórmula NER= 70 x (peso en kg)0,75).
En los pacientes con sepsis es frecuente que la regulación de la glucemia esté alterada, observándose una hiperglucemia en estadios muy iniciales, seguida de hipoglucemia a medida que empeora la gravedad de la enfermedad. Se recomienda mantener la glucemia en 70-140 mg/dl. En pacientes hipoglucémicos se debe administrar un bolo intravenoso de glucosa (0,5-1,0 ml/kg de glucosa diluida al 50%). Si la respuesta al bolo es transitoria, los fluidos de mantenimiento se pueden suplementar con glucosa (2,5-5%). Cuando la glucemia es superior a 150 mg/dl de forma sostenida, se puede iniciar la administración de insulina regular en infusión constante (0,05-0,1 UI/kg/h), monitorizando la concentración de glucosa en sangre de forma intensiva.
Rafael Obrador de Aguilar
El pronóstico del paciente con sepsis depende de la gravedad de la afección, la causa subyacente inicial y la presencia o ausencia de disfunción orgánica. En perros con sepsis no complicada, el pronóstico es bueno, con una tasa de supervivencia de en torno al 84%. Sin embargo, una vez que el animal empieza a desarrollar disfunción orgánica o presenta shock séptico, el pronóstico empeora notablemente. De hecho, la mortalidad está claramente asociada a la disfunción orgánica, aumentando con el número de sistemas orgánicos afectados 17. Sin embargo, la lesión tisular no tiene por qué ser irreversible y puede resolverse de forma parcial o total si la causa subyacente de la inflamación se trata con éxito.
La sepsis es una urgencia médica cuyo pronóstico depende de la rapidez con que se realicen ciertos procedimientos, tanto para el diagnóstico como para el tratamiento del paciente. El paciente se debe evaluar y revaluar las veces necesarias, ya que se encuentra en una situación de constante evolución y requiere un estrecho seguimiento de la respuesta al tratamiento.
Funk DJ, Parrillo JE, Kumar A. Sepsis and septic shock: a history. Crit. Care Clin. 2009;125(1):83-101.
Bone RC, Balk RA, Cerra FB, et al. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis: the ACCP/SCCM consensus conference committee. American College of Chest Physicians/Society of Critical Care Medicine. Chest 1992;101(6): 1644-1655.
Greiner M, Wolf G, Hartmann K. A retrospective study of the clinical presentation of 140 dogs and 39 cats with bacteraemia. J. Small Anim. Pract. 2008;49(8):378-383.
Bonczynski JJ, Ludwig LL, Barton LJ, et al. Comparison of peritoneal fluid and peripheral blood pH, bicarbonate, glucose, and lactate concentration as a diagnostic tool for septic peritonitis in dogs and cats. Vet. Surg. 2003;32(2):161-166.
Leisman DE, Doerfler ME, Schneider SM, et al. Predictors, prevalence, and outcomes of early crystalloid responsiveness among initially hypotensive patients with sepsis and septic shock. Crit. Care Med. 2018;46(2):189-198.
Morley PT. Early fluid management in sepsis: yes. Crit. Care Med. 2018;46(2):327-328.
Ospina-Tascon G, Neves AP, Occhipinti G, et al. Effects of fluids on microvascular perfusion in patients with severe sepsis. Intens. Care Med. 2010;36(6):949-955.
Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intens. Care Med. 2017;43:304-377.
Rausei S, Pappalardo V, Ruspi L, et al. Early versus delayed source control in open abdomen management for severe intra-abdominal infections: a retrospective analysis on 111 cases. World J. Surg. 2018;42(3):707-712.
Hardie, E. Therapeutic management of sepsis. In; Bonagura J (ed): Kirk´s Current Veterinary Therapy: XIII Small Animal Practice Philadelphia: WB Saunders, 2000;272-275.
Cecconi M, De Backer D, Antonelli M, et al. Consensus on circulatory shock and hemodynamic monitoring. Task Force of the European Society of Intensive Care Medicine. Intens. Care Med. 2014;40(12):1795-1815.
Ospina-Tascón G, Hernandez G, Alvarez I, et al. Effects of very early start of norepinephrine in patients with septic shock: a propensity score-based analysis. Crit. Care 2020;24(1):52.
Kimmoun A, Ducrocq N, Levy B. Mechanisms of vascular hyporesponsiveness in septic shock. Curr. Vasc. Pharmacol. 2013;11:139-149.
Annane D, Pastores SM, Rochwerg B, et al. Guidelines for the diagnosis and management of critical illness-related corticosteroid insufficiency (CIRCI) in critically ill patients (part I): Society of Critical Care Medicine (SCCM) and European Society of Intensive Care Medicine (ESICM) 2017. Intens. Care Med. 2017;43:1751-1763.
Pastores SM, Annane D, Rochwerg B. Corticosteroid Guideline Task Force of SCCM and ESICM. Guidelines for the diagnosis and management of critical illness-related corticosteroid insufficiency (CIRCI) in critically ill patients (part II): Society of Critical Care Medicine (SCCM) and European Society of Intensive Care Medicine (ESICM) 2017. Crit. Care Med. 2018;46:146-148.
Summers AM, Culler C, Yaxley PE, et al. Retrospective evaluation of the use of hydrocortisone for treatment of suspected critical illness-related corticosteroid insufficiency (CIRCI) in dogs with septic shock (2010-2017): 47 cases. J. Vet. Emerg. Crit. Care 2021;31:371-379.
Kenney EM, Rozanski EA, Rush JE, et al. Association between outcome and organ system dysfunction in dogs with sepsis: 114 cases (2003-2007). J. Am. Vet. Med. Assoc. 2010;236(1):83-87.
Rafael Obrador de Aguilar
El Dr. Obrador es licenciado en veterinaria por la Universidad de Zaragoza Leer más
¿Estás pensando en hacer un internado en Estados Unidos? Este artículo resume brevemente las posibles ventajas y desventajas de estos programas de formación.
Prescribir fluidoterapia intravenosa en el gato no es tan sencillo como puede parecer; este artículo proporciona una visión general de los conocimientos actuales.
El fallo cardiaco agudo en el perro conlleva el riesgo de muerte, por lo que, tal y como indica Luca Ferasin, es esencial optimizar el diagnóstico y el tratamiento.
¿Qué podemos hacer cuando un paciente diabético en estado crítico llega a urgencias? Este artículo describe paso a paso el enfoque a seguir para obtener el resultado óptimo.
