Faire un internat vétérinaire aux États-Unis
Vous envisagez de faire un internat aux États-Unis ? Cet article présente brièvement les avantages et les inconvénients de ce type de projet.
Numéro du magazine 32.3 Autre scientifique
Publié 12/04/2023
Aussi disponible en Deutsch , Italiano , Español et English
Le sepsis est une urgence médicale chez le chien dont le pronostic dépend essentiellement de la rapidité du diagnostic et d’une intervention proactive.

La présence d’un sepsis doit être considérée comme une urgence médicale dont l’issue dépend beaucoup de la rapidité du diagnostic.
Une réanimation rapide et adéquate peut permettre d’empêcher qu’un sepsis ne conduise à une défaillance multiviscérale et au choc septique.
Une antibiothérapie s’avère indispensable lors de suspicion de sepsis chez un chien qui présente des signes de choc.
Évaluer, réévaluer et encore réévaluer : le sepsis est une affection qui évolue constamment et dont la réponse au traitement doit être activement surveillée.
Le sepsis est une urgence médicale connue depuis l’époque d’Hippocrate, vers 400 ans avant J.C. : il était associé à toutes les maladies provoquant la putréfaction de la viande. Environ 1 400 ans plus tard, Avicenne, un médecin perse, a décrit le sepsis comme une putréfaction du sang et des tissus, accompagnée de fièvre 1. Aujourd’hui, nous savons que cette affection est une maladie généralisée due à une réponse inappropriée du système immunitaire confronté à un agent infectieux. Le sepsis peut entraîner la défaillance d’un ou plusieurs organes, et c’est la cause la plus fréquente de mortalité chez les chiens présentant un sepsis. Un diagnostic précoce et une intervention thérapeutique efficace sont donc extrêmement importants.
En 1991, la médecine moderne a donné une définition du sepsis (connue sous le nom de Sepsis - 1), et bien qu’elle ait évolué depuis (Sepsis - 2 et - 3), les concepts originels utilisés en pratique vétérinaire sont toujours les mêmes 2. La définition cherchait au départ à standardiser les critères et à établir des lignes directrices pour aider à reconnaître et à traiter les animaux atteints de sepsis le plus rapidement et le plus efficacement possible. Ces concepts figurent ci-dessous :
Tableau 1. Critères d’identification d’un SRIS chez le chien.
| Température (°C) | ≤ 37,2 or ≥ 39,2 |
| Fréquence cardiaque (battements/mn) | ≥ 140 |
| Fréquence respiratoire (cycles/mn) | > 20 |
| Numération leucocytaire (x 103/µL) | ≥ 16 ou ≤ 6 |
| Polynucléaires de type “Band”* (%) | ≥ 3 |
*Aspect de polynucléaires neutrophiles mais le noyau est allongé, sans lobes nets (les pincements du noyau ont une épaisseur < à la moitié de l’épaisseur du noyau).
Bien comprendre la pathogénie du SRIS est essentiel. Le SRIS constitue une réponse systémique à tout trouble provoquant une inflammation, qui peut soit être généralisée d’emblée (comme chez un animal victime d’un coup de chaleur), soit localisée (comme en cas de pancréatite aiguë). La réponse inflammatoire de l’organisme ne peut pas être cantonnée au foyer initial, si bien que l’état inflammatoire se généralise et commence à affecter des tissus normaux situés dans des zones éloignées n’ayant aucun lien avec la cause initiale. Par conséquent, et quelle que soit l’origine du problème, tous les systèmes organiques peuvent présenter des signes d’inflammation. Si la cause initiale est infectieuse, l’animal est défini comme septique ; en d’autres termes, tous les animaux septiques présentent une inflammation systémique (c’est-à-dire un SRIS), mais tous les cas de SRIS ne sont pas d’origine infectieuse comme c’est le cas lors de traumatismes, de coup de chaleur ou de pancréatite.
Tableau 2. Définitions d’une défaillance viscérale chez le chien.
| Système organique | Critères |
|---|---|
| Rénal |
Débit urinaire < 0,5 mL/kg/h depuis plus de 12 heures ou augmentation de la créatinine sérique ≥ 0,3 mg/dL sans signe d’azotémie pré- ou post-rénale
|
| Cardiovasculaire |
Hypotension nécessitant l’utilisation de vasopresseurs
|
| Respiratoire |
Nécessité d’administrer de l’oxygène ou une ventilation assistée sur la base de l’évaluation clinique et des gaz artériels : gradient alvéolaire – artériel > 10 mmHg ou oxymétrie de pouls (SpO2 < 95 %)
|
| Hépatique |
Bilirubine totale sérique ou plasmatique > 0,5 mg/dL
|
| Coagulation |
Temps de prothrombine ou temps de thromboplastine partielle activée > 25 % du seuil supérieur de référence ou numération plaquettaire ≤ 100 000/µL
|
En se basant sur les éléments exposés ci-dessus, la première étape consiste à savoir si le chien présente une réponse inflammatoire systémique. Les critères utilisés à cet effet incluent les modifications de la fréquence respiratoire (tachypnée), de la fréquence cardiaque (bradycardie ou tachycardie), de la température rectale (hypothermie ou fièvre), ainsi que des anomalies des paramètres sanguins (leucopénie ou leucocytose avec ou sans décalage vers la gauche) (Tableau 1). La présence d’au moins deux de ces critères est suffisante pour confirmer un SRIS chez un chien 3. La valeur diagnostique de ces critères réside dans leur simplicité ; il n’est pas nécessaire de recourir à des examens plus sophistiqués et cela permet d’identifier rapidement un animal atteint. Ces critères ne sont cependant pas spécifiques et le plus grand problème réside dans le fait que la plupart des animaux hospitalisés dans une structure vétérinaire répondent à une ou plusieurs des conditions du SRIS. En règle générale, la probabilité de SRIS augmente quand même avec le nombre de conditions remplies. Un SRIS est beaucoup plus probable chez chien présentant une tachycardie, une tachypnée, de la fièvre et une leucocytose, que chez un chien présentant seulement une tachycardie et une tachypnée, ces signes cliniques pouvant être déclenchés par le stress et l’anxiété du séjour à la clinique.
L’étape suivante cherchera à établir, en s’appuyant avant tout sur les commémoratifs et l’examen clinique, si l’origine du SRIS est infectieuse (c’est-à-dire un sepsis) ou pas (Figure 1). Dans certains cas (si par exemple un abcès cutané s’est développé à la suite d’une morsure), il est facile de repérer la cause initiale. D’autres cas sont plus délicats et nécessitent des examens approfondis. Chaque fois qu’un sepsis est suspecté, il est toujours souhaitable d’effectuer au moins un bilan sanguin complet (hématologique et biochimique) et des analyses urinaires (incluant une culture). Les résultats du bilan sanguin peuvent par exemple indiquer la présence d’une leucocytose ou d’une leucopénie, d’une thrombocytopénie, d’une hypoalbuminémie, d’une hyperbilirubinémie, d’une hypocalcémie, d’une azotémie et d’une hyper- ou hypoglycémie : ce sont les anomalies les plus fréquemment observées chez les chiens septiques. Ce bilan initial peut être complété par d’autres examens visant à rechercher un foyer infectieux, notamment une radiographie thoracique, abdominale ou vertébrale (Figure 2), une échographie abdominale ou thoracique, et d’autres techniques d’imagerie pourront être utilisées si elles sont disponibles (Figure 3). En fonction de la présentation clinique et de la situation géographique, une ponction du liquide céphalorachidien ou articulaire, une sérologie ou une PCR pour rechercher une maladie infectieuse pourront être réalisées. En règle générale, tout épanchement liquidien anormal doit être ponctionné et analysé à la cytologie car la présence de bactéries intracellulaires confirmera l’infection ; un échantillon sera aussi conservé pour une éventuelle culture ultérieure et un antibiogramme si nécessaire (Figure 4). Si une péritonite septique est suspectée chez un chien mais qu’aucune bactérie intracellulaire n’est retrouvée dans le liquide péritonéal, la glycémie sera comparée à la concentration en glucose dans le liquide péritonéal : une différence supérieure à 20 mg/dL (sang > liquide péritonéal) est compatible avec un diagnostic de péritonite septique 4. Bien qu’une cause infectieuse puisse être suspectée dès l’examen initial, il n’est cependant pas toujours possible de la confirmer. Le vétérinaire doit donc envisager d’autres possibilités ou surveiller la réponse au traitement en réévaluant fréquemment l’état de l’animal.

Figure 1. Muqueuses orales congestionnées chez un chien atteint de SRIS.
© Rocio Redondo

Figure 2. Radiographie thoracique latérale d’un chien victime d’une pneumonie par aspiration. Noter la présence de bronchogrammes aériques dans les lobes pulmonaires crâniaux droit et gauche, ainsi que dans le lobe moyen droit ; l’œsophage présente également une dilatation aérique généralisée.
© Rafael Obrador de Aguilar
La présentation clinique d’un chien atteint de sepsis peut beaucoup varier et, si certains animaux nécessitent des soins intensifs pour survivre, d’autres peuvent être traités en ambulatoire. La stabilisation de ces animaux dépend surtout de la qualité de la réanimation, du contrôle de l’origine de l’infection, de l’antibiothérapie et de l’utilisation de vasopresseurs (en cas de choc septique).
 |
| a |
 |
| b |
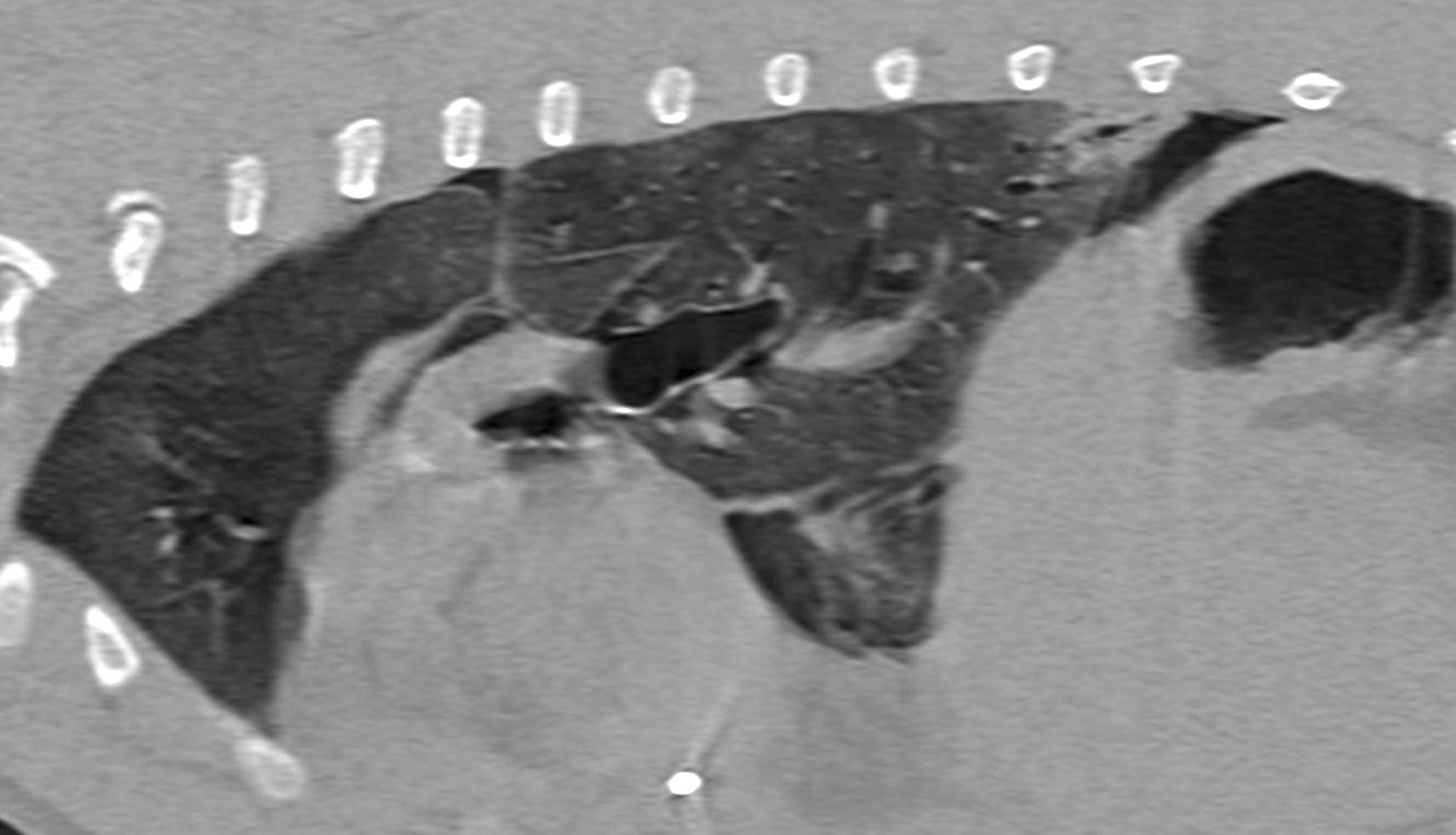
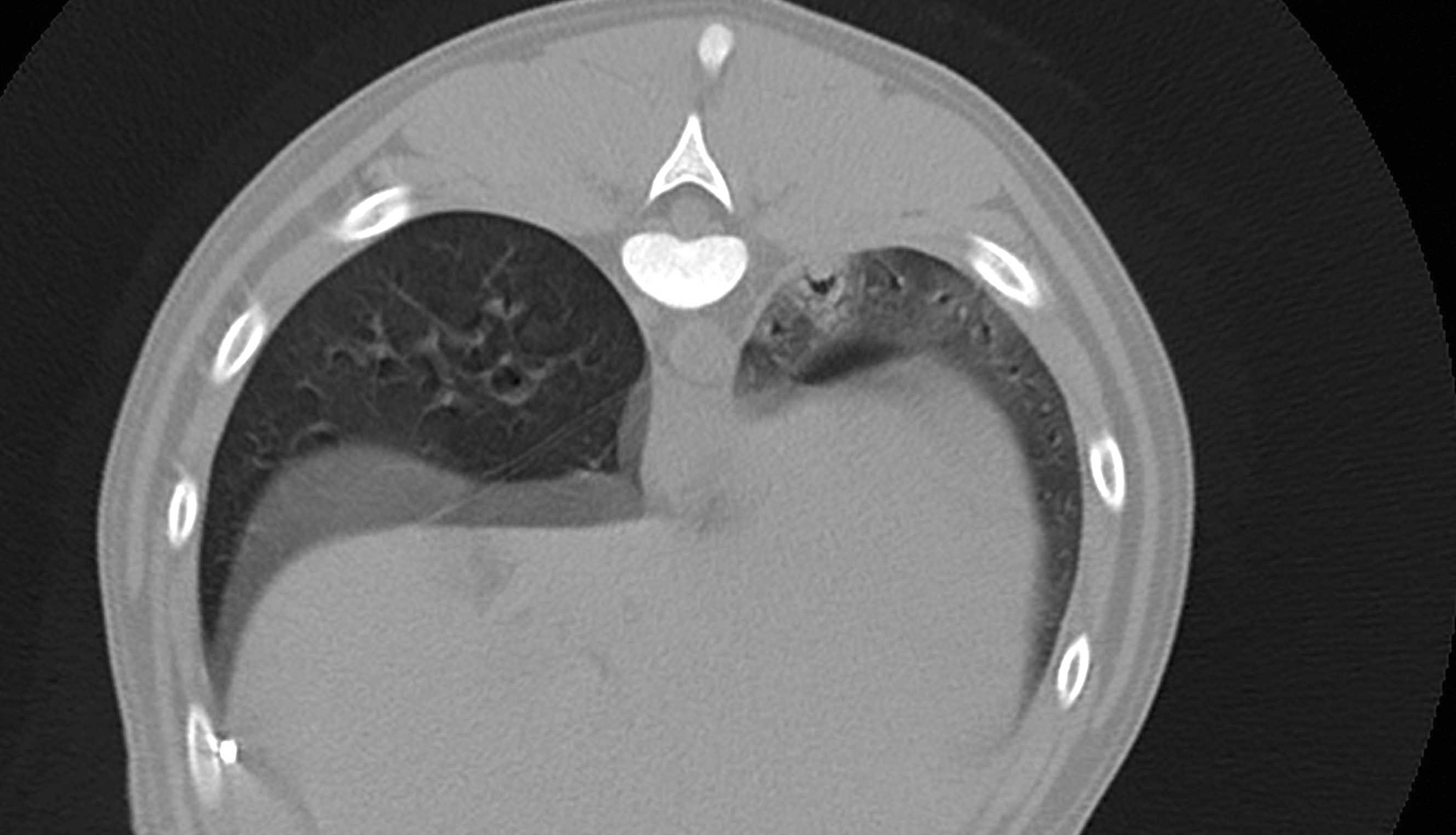
Figure 3. Vues sagittale (a) et transversale (b) obtenues au scanner d’un chien atteint de sepsis et présentant un pyothorax secondaire à la migration d’une épine végétale. Le lobe pulmonaire caudal gauche est repoussé de la paroi thoracique et présente une opacification alvéolaire localisée ; un petit bronchogramme aérique est également visible.
© Rafael Obrador de Aguilar
La réanimation d’un chien atteint de sepsis diffère de celle des animaux présentant d’autres formes de choc. Dans le cas du sepsis, la défaillance hémodynamique résulte de la combinaison d’une hypovolémie absolue (qui bénéficie de la fluidothérapie) et d’une hypovolémie relative consécutive à l’augmentation de la perméabilité vasculaire qui entraîne des pertes liquidiennes, une baisse du tonus vasculaire et (chez certains chiens) un dysfonctionnement du myocarde. Chacun de ces facteurs peut affecter l’individu à un degré très variable au cours du temps et une approche thérapeutique standard ne peut logiquement pas également profiter à tous les chiens. Il est donc préférable d’ajuster le protocole de fluidothérapie en fonction des besoins de chaque animal.
 |
 |
| a | b |
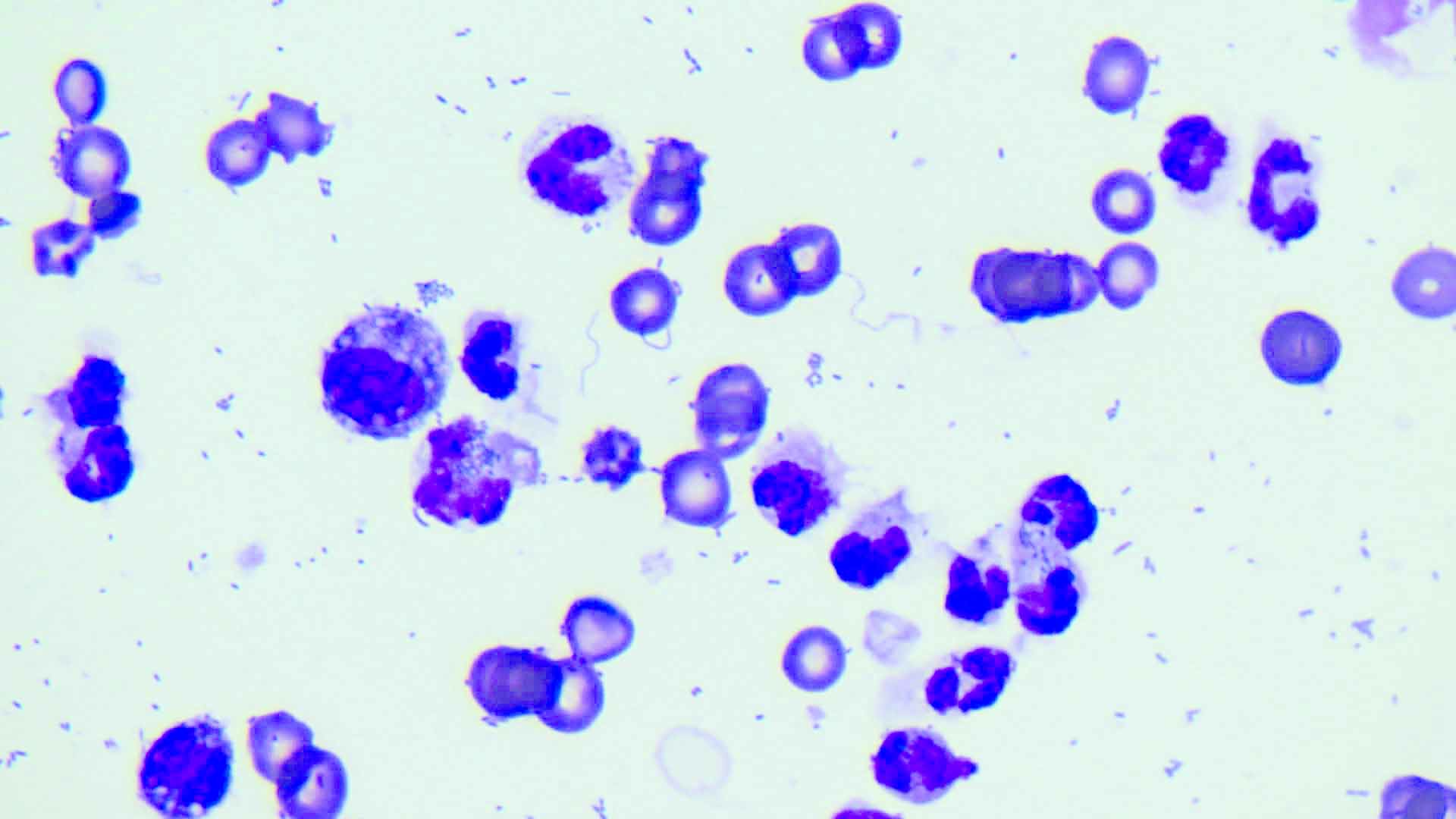
Figure 4. (a) Prélèvement réalisé par abdominocentèse chez un chien présentant un abdomen septique. (b) L’analyse cytologique du liquide montre la présence de bactéries intracellulaires (grossissement x 100).
© Rafael Obrador de Aguilar
Actuellement, aucun protocole de fluidothérapie (type, volume et fréquence d’administration du soluté) n’a montré de supériorité pour traiter les animaux septiques mais la vitesse de sa mise en œuvre, une fois les troubles hémodynamiques détectés, est très importante. Dans la mesure du possible, le délai ne devrait pas dépasser 20 à 30 minutes. En effet, un apport liquidien précoce peut moduler l’état inflammatoire et même réduire le besoin de vasopresseurs (Figure 5) ; en revanche, une administration tardive ou inadéquate est associée à une aggravation de l’état hémodynamique, du débit sanguin dans la microcirculation et de la défaillance viscérale 5,6,7. Il est donc recommandé de commencer la réanimation avec un cristalloïde isotonique équilibré (par exemple, du Ringer lactate) 8. Un bolus intraveineux (10-20 mL/kg sur environ 15 minutes) pourra généralement être administré tout en surveillant les paramètres de perfusion (c’est-à-dire l’état de vigilance, la fréquence cardiaque, la couleur des muqueuses, le temps de remplissage capillaire, la température des extrémités et la qualité du pouls) ; l’objectif est d’améliorer ou même de normaliser ces paramètres. Si la réponse du chien n’est pas favorable (c’est-à-dire que les paramètres de perfusion ne s’améliorent pas), un bolus de fluide sera réadministré deux ou trois fois, tout en vérifiant que rien ne signale une éventuelle surcharge volumique : tremblements, nausées, respiration sifflante, chémosis, écoulement nasal séreux, augmentation de la fréquence ou des efforts respiratoires, œdème sous-cutané, crépitants à l’auscultation pulmonaire… Tous ces signes constituent une contre-indication pour continuer la fluidothérapie qui risque alors de devenir dangereuse.
Une fois le chien réanimé, le protocole d’administration de la fluidothérapie sera adapté (comme pour tout animal en soins intensifs) à l’état de déshydratation du chien, à ses besoins d’entretien et à la présence d’éventuelle pertes liquidiennes chroniques. Environ 15 % des chiens atteints de sepsis évoluent cependant vers un choc septique, qui se caractérise par une insuffisance circulatoire, une défaillance multiviscérale et une mortalité accrue. À ce stade, même une fluidothérapie adéquate ne peut plus inverser l’hypotension générale qui en résulte, et l’administration de vasopresseurs (voir ci-dessous) devient incontournable.

Figure 5. Chez un chien en choc septique, l’administration de la fluidothérapie doit démarrer dès que possible, en utilisant un cristalloïde isotonique équilibré.
© Shutterstock
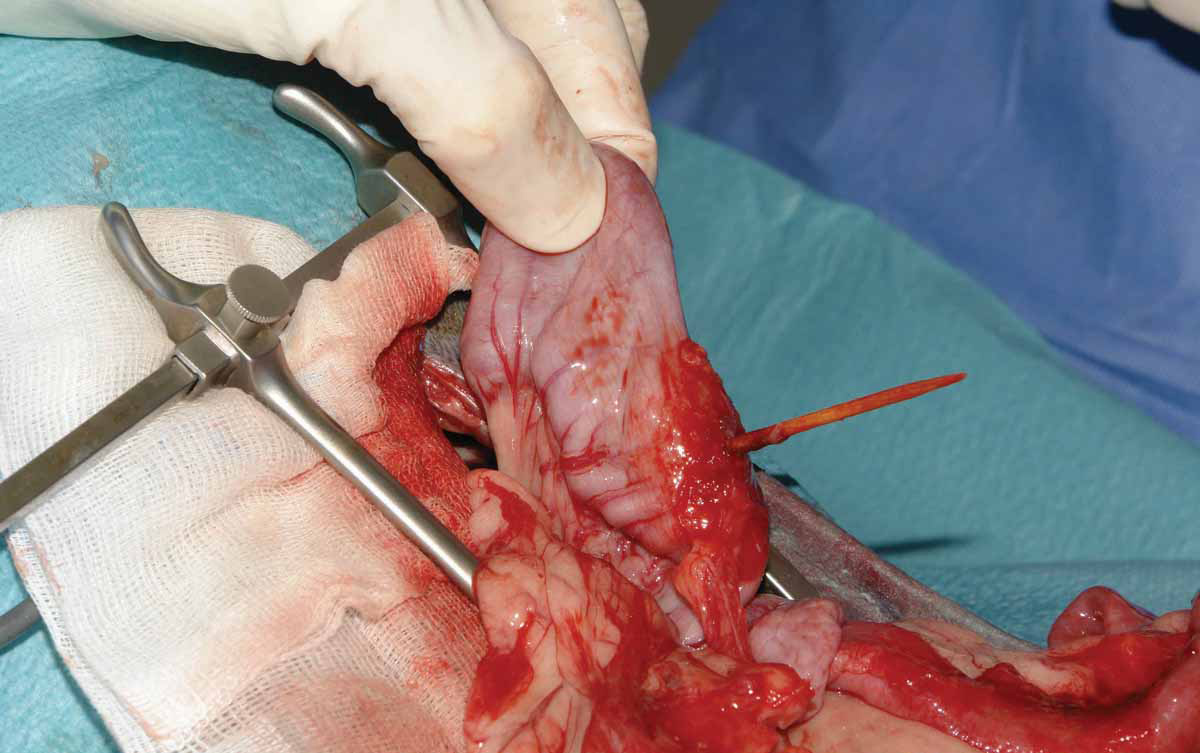
Contrôler le foyer infectieux permet d’éliminer la cause initiale et de prévenir l’évolution possible vers une défaillance viscérale chez les chiens atteints de sepsis. Par conséquent, une fois la réanimation réalisée, il est essentiel de drainer ou de faire l’ablation chirurgicale du tissu infecté le plus vite possible car l’élimination précoce et adéquate du foyer infectieux influence positivement le pronostic (Figure 6) 9. Cette étape permet également de faire des prélèvements destinés à l’analyse microbiologique.
 |
| a |
 |
| b |
 |
| c |
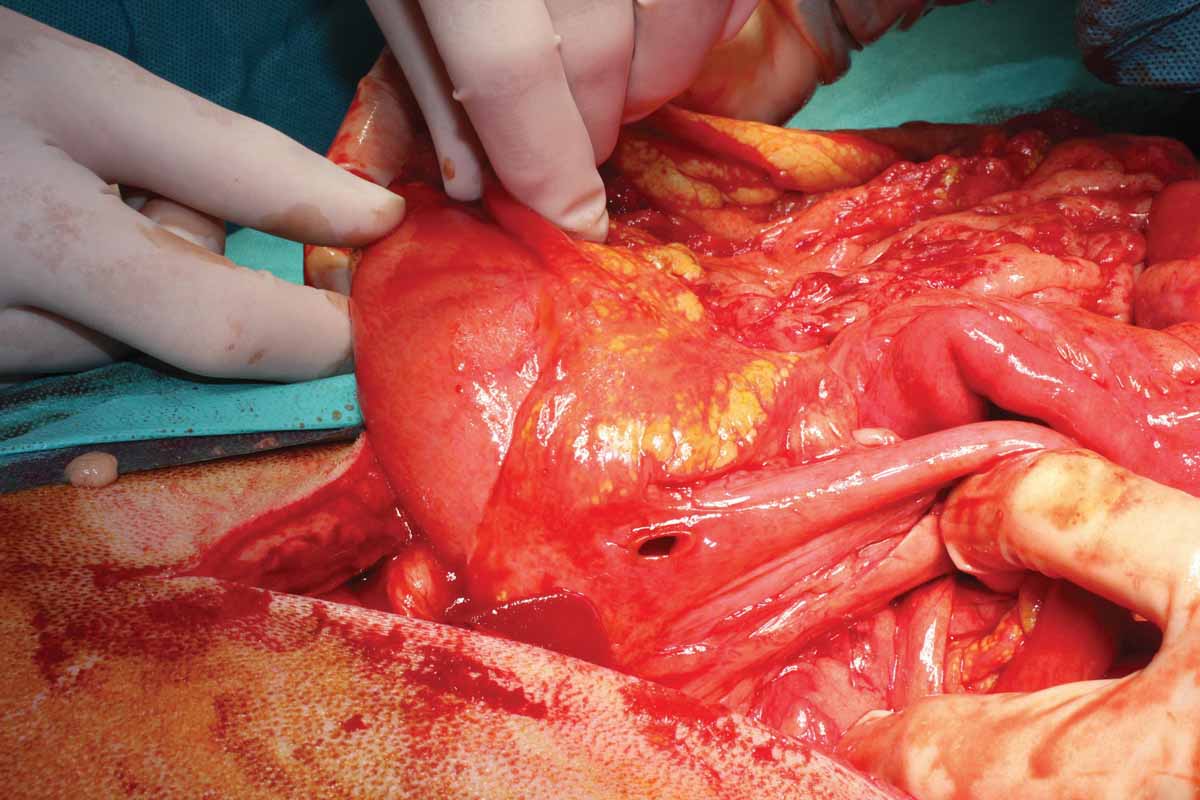
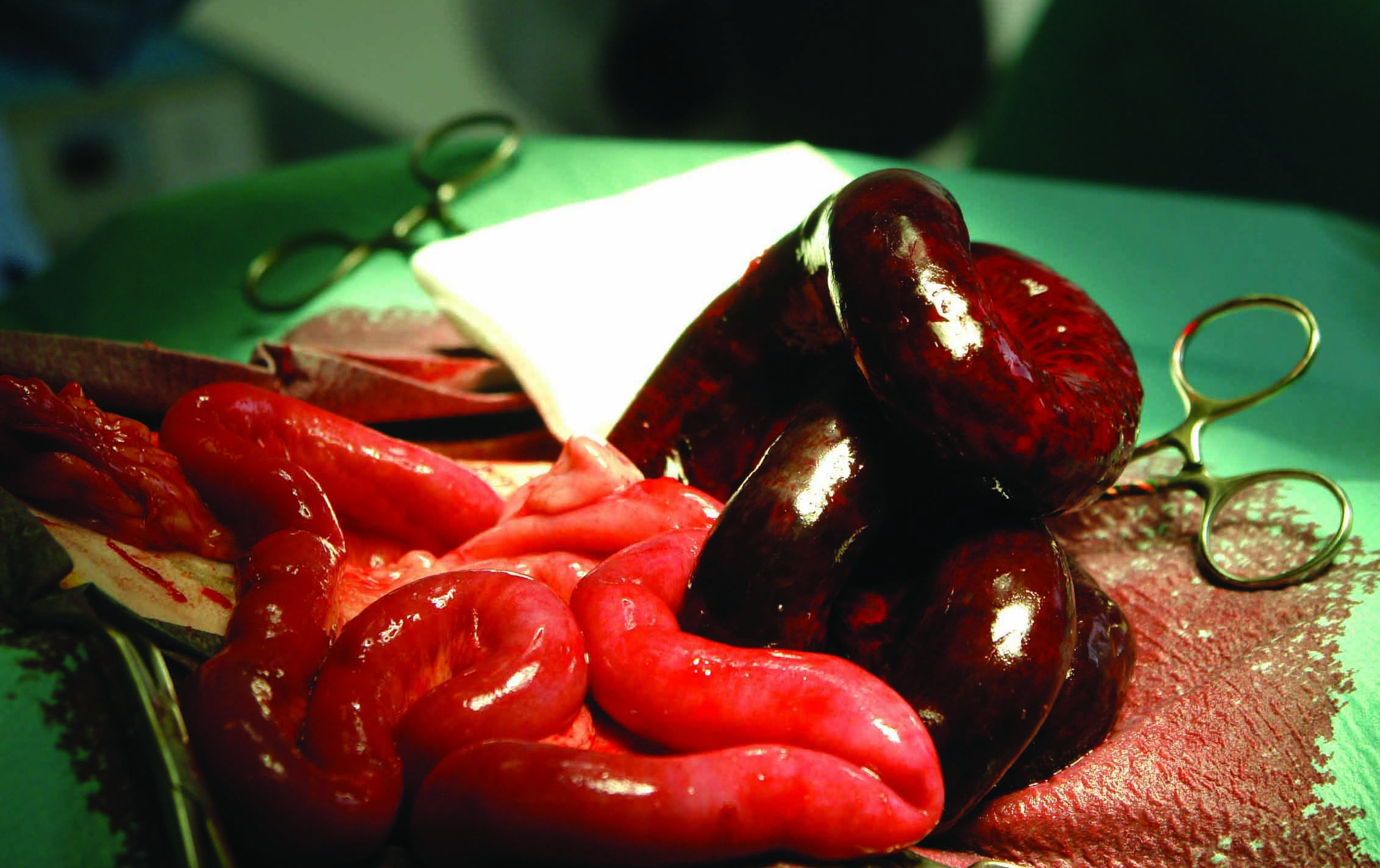
Figure 6. Exemples d’abdomen septique : (a) perforation duodénale consécutive à un traitement par des anti-inflammatoires non stéroïdiens ; (b) perforation intestinale due à un corps étranger ; (c) torsion mésentérique.
© Nuria Vizcaíno
Une antibiothérapie précoce et adaptée constitue l’un des principaux piliers du traitement du sepsis, en particulier pour les chiens dont l’état est le plus critique, tels que ceux qui présentent une défaillance viscérale ou un choc septique. Dans la mesure du possible, et si cela ne retarde pas le démarrage de l’antibiothérapie, il est conseillé de faire des prélèvements destinés à la culture et à l’antibiogramme. En attendant les résultats des analyses, il faut traiter empiriquement avec un antibiotique à large spectre, susceptible d’agir efficacement contre les germes potentiellement en cause dans le sepsis. D’autres facteurs seront aussi pris en compte, notamment l’état du chien (qui conditionne par exemple l’administration de l’antibiotique par voie orale ou intraveineuse) et la possibilité d’infections multirésistantes (dues à une exposition antérieure aux antibiotiques, à une hospitalisation récente ou à une contamination nosocomiale). La dose administrée devra être suffisante pour éliminer l’agent pathogène, tout en minimisant les risques de développement de résistances bactériennes et en évitant les effets indésirables. Quelques exemples de polythérapie suivent ; ils concernent des chiens atteints de sepsis qui doivent être hospitalisés et n’ayant pas reçu d’antibiotiques dans les semaines précédant leur admission 10:
Le traitement empirique choisi pourra ensuite changer en fonction de l’évolution de l’état du chien et des résultats de la culture et de l’antibiogramme ; ce processus est appelé la désescalade. Il s’agit de limiter le spectre et le nombre d’antibiotiques au minimum nécessaire pour bien contrôler l’infection une fois le germe en cause identifié. Cela s’inscrit dans une démarche rationnelle d’utilisation des antibiotiques, qui minimise les risques d’effets secondaires et contribue à prévenir l’antibiorésistance.
Si une hypotension systémique (pression artérielle systolique < 90 mmHg) est détectée chez un chien septique qui ne répond pas à la fluidothérapie (choc septique), un traitement vasopresseur doit être mis en place dès que possible 11. L’introduction précoce des vasopresseurs chez les animaux en choc septique est associée à un volume plus faible de liquides administrés pendant la réanimation, à moins de rétention liquidienne dans les tissus et à une durée plus courte de l’hypotension, ce qui pourrait réduire la mortalité des animaux 12. L’objectif est d’essayer d’augmenter les résistances vasculaires périphériques et d’améliorer la pression artérielle pour maintenir une perfusion correcte des organes vitaux. Si le chien avait auparavant une pression artérielle normale, la pression systolique sera maintenue au-dessus de 90-100 mmHg.
Les deux vasopresseurs les plus utilisés en médecine vétérinaire sont la noradrénaline (norépinéphrine) et la dopamine (Tableau 3). La noradrénaline est une catécholamine qui augmente la pression artérielle principalement en raison de ses propriétés vasoconstrictrices, avec un effet minimal sur la fréquence cardiaque (effet α 1 marqué et effet β 1 modéré). De plus, grâce à une réanimation volumique adéquate, le débit sanguin rénal s’améliore et le taux de lactate diminue. La dopamine est le précurseur naturel de la noradrénaline dans l’organisme mais ses effets sont légèrement différents et dépendent de la dose. Par rapport à la noradrénaline, une dose intermédiaire (3-10 µg/kg/min) produit généralement des effets plus marqués sur le cœur (β 1) et plus faibles sur les vaisseaux (α 1) ; le risque de tachycardie ou d’arythmies est donc plus important et ce médicament est moins souvent utilisé que la noradrénaline. Le choix dépend cependant des préférences personnelles et de l’expérience du praticien.
Tableau 3. Les vasopresseurs chez le chien : mécanisme d’action et doses recommandées.
| Vasopresseurs | α | β1 | β2 |
Contractibilité | Rythme cardiaque | Tonus vasculaire | Pression artérielle | Posologie |
|---|---|---|---|---|---|---|---|---|
| Dobutamine | + | + | ++ | ↑↑ | ↑ | ↓ | Variable | 5-20 µg/kg/mn |
| Dopamine | ++ | + | ++ | ↑↑ | ↑↑ | ↑↑ | ↑↑ | 5-20 µg/kg/mn |
| Adrénaline | +++ | +++ | +++ | ↑↑↑ | ↑↑↑ | ↑↑↑ | ↑↑↑ | 0,05-1,0 µg/kg/mn |
| Noradrénaline | +++ | + | 0 | ↑ | Variable | ↑↑↑ | ↑↑↑ | 0,1-2,0 µg/kg/mn |
| Vasopressine | 0 | 0 | 0 | 0 | ↓ | ↑↑ | ↑↑ |
0,5-5,0 mU/kg/mn
|
Les deux médicaments seront administrés par voie intraveineuse, grâce à une perfusion continue, en démarrant au bas de la fourchette posologique recommandée et en augmentant progressivement jusqu’à ce que le chient soit stabilisé sur le plan hémodynamique (pression systolique > 90-100 mmHg). Chez certains chiens présentant un choc septique, la fluidothérapie et de fortes doses de vasopresseurs ne permettent cependant pas d’améliorer l’hypotension ; cette situation est qualifiée de choc réfractaire 13. Dans ce cas, le chien doit être réexaminé et les causes possibles du choc réfractaire seront recherchées (Tableau 4).
Tableau 4. Causes d’un choc réfractaire.
|
L’administration de glucocorticoïdes n’est pas recommandée chez les chiens septiques si la stabilité hémodynamique peut être maintenue grâce à la fluidothérapie ou à des vasopresseurs. L’administration de corticostéroïdes sera cependant envisagée chez un chien en choc septique qui ne répond pas au traitement liquidien et chez qui l’hypotension persiste malgré de fortes doses de catécholamines 14,15. Ce type de médicaments augmente la réponse vasculaire adrénergique et réduit la vasodilatation liée à l’inflammation. Les protocoles recommandés comprennent l’administration d’un bolus intraveineux d’hydrocortisone (1 mg/kg suivi d’une perfusion continue à 0,08 mg/kg/h 16) ou de dexaméthasone (en utilisant une perfusion continue de 0,01-0,02 mg/kg/h).
Le tube digestif est considéré comme l’organe cible du choc dans l’espèce canine ; il est très sensible aux problèmes d’hypoperfusion car, en situation critique, le flux sanguin est détourné vers des organes nobles. Cet effet est renforcé par l’existence d’une anorexie et peut altérer de manière significative la perméabilité de la barrière gastro-intestinale ; une translocation bactérienne (ou d’endotoxines) devient alors possible. Comme les chiens septiques anorexiques sont aussi particulièrement sensibles à la malnutrition, il est très important de commencer à les nourrir le plus tôt possible ; le chien doit cependant être d’abord réhydraté et stable sur le plan hémodynamique, et ne pas présenter de déséquilibres électrolytiques importants. L’alimentation peut être spontanée mais, si le chien est anorexique, il sera nourri par sonde. Le premier objectif est d’apporter des nutriments aux entérocytes pour maintenir la barrière gastro-intestinale fonctionnelle ; au départ, la ration peut donc être inférieure au besoin énergétique au repos (BER) du chien (évalué à 70 x (poids en kg)0,75).
Des perturbations de la régulation de la glycémie sont fréquemment observées chez les chiens septiques : une hyperglycémie peut apparaître en début d’évolution mais une hypoglycémie lui succède lorsque la situation s’aggrave. Il est recommandé de maintenir la glycémie entre 70 et 140 mg/dL. Pour les chiens hypoglycémiques, un bolus intraveineux de glucose sera administré (0,5-1,0 mL/kg de glucose dilué à 50 %). Si la réponse au bolus n’est pas durable, du glucose (2,5-5 %) sera inclus dans la fluidothérapie d’entretien. Lorsque la glycémie dépasse régulièrement 150 mg/dL, de l’insuline standard pourra être administrée via une perfusion continue (0,05-0,1 UI/kg/h), en surveillant attentivement l’évolution de la glycémie.
Rafael Obrador de Aguilar
Chez un chien septique, le pronostic dépend de la gravité de l’affection, de la cause initiale sous-jacente et de la présence ou de l’absence de défaillance viscérale. Chez un chien présentant un sepsis non compliqué, le pronostic est bon, et le taux de survie avoisine 84 %. En revanche, le pronostic est nettement dégradé si l’animal commence à présenter une défaillance viscérale ou que le choc septique s’installe. En pratique, la mortalité est clairement associée à la défaillance viscérale et augmente avec le nombre d’organes touchés 17. Les lésions tissulaires ne sont cependant pas forcément irréversibles et peuvent disparaître partiellement ou totalement si la cause sous-jacente de l’inflammation est traitée avec succès.
Le sepsis est une urgence médicale dont le pronostic dépend de la rapidité avec laquelle certaines procédures sont entreprises, tant au niveau diagnostique que thérapeutique. L’état du chien doit être évalué et réévalué aussi souvent que nécessaire car cette affection se modifie en permanence et exige de surveiller étroitement la réponse au traitement.
| Remerciements aux Dres Céline Pouzot-Névoret et Alexandra Nectoux pour la relecture attentive de la version française de cet article. |
Funk DJ, Parrillo JE, Kumar A. Sepsis and septic shock: a history. Crit. Care Clin. 2009;125(1):83-101.
Bone RC, Balk RA, Cerra FB, et al. Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis: the ACCP/SCCM consensus conference committee. American College of Chest Physicians/Society of Critical Care Medicine. Chest 1992;101(6): 1644-1655.
Greiner M, Wolf G, Hartmann K. A retrospective study of the clinical presentation of 140 dogs and 39 cats with bacteraemia. J. Small Anim. Pract. 2008;49(8):378-383.
Bonczynski JJ, Ludwig LL, Barton LJ, et al. Comparison of peritoneal fluid and peripheral blood pH, bicarbonate, glucose, and lactate concentration as a diagnostic tool for septic peritonitis in dogs and cats. Vet. Surg. 2003;32(2):161-166.
Leisman DE, Doerfler ME, Schneider SM, et al. Predictors, prevalence, and outcomes of early crystalloid responsiveness among initially hypotensive patients with sepsis and septic shock. Crit. Care Med. 2018;46(2):189-198.
Morley PT. Early fluid management in sepsis: yes. Crit. Care Med. 2018;46(2):327-328.
Ospina-Tascon G, Neves AP, Occhipinti G, et al. Effects of fluids on microvascular perfusion in patients with severe sepsis. Intens. Care Med. 2010;36(6):949-955.
Rhodes A, Evans LE, Alhazzani W, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intens. Care Med. 2017;43:304-377.
Rausei S, Pappalardo V, Ruspi L, et al. Early versus delayed source control in open abdomen management for severe intra-abdominal infections: a retrospective analysis on 111 cases. World J. Surg. 2018;42(3):707-712.
Hardie, E. Therapeutic management of sepsis. In; Bonagura J (ed): Kirk´s Current Veterinary Therapy: XIII Small Animal Practice Philadelphia: WB Saunders, 2000;272-275.
Cecconi M, De Backer D, Antonelli M, et al. Consensus on circulatory shock and hemodynamic monitoring. Task Force of the European Society of Intensive Care Medicine. Intens. Care Med. 2014;40(12):1795-1815.
Ospina-Tascón G, Hernandez G, Alvarez I, et al. Effects of very early start of norepinephrine in patients with septic shock: a propensity score-based analysis. Crit. Care 2020;24(1):52.
Kimmoun A, Ducrocq N, Levy B. Mechanisms of vascular hyporesponsiveness in septic shock. Curr. Vasc. Pharmacol. 2013;11:139-149.
Annane D, Pastores SM, Rochwerg B, et al. Guidelines for the diagnosis and management of critical illness-related corticosteroid insufficiency (CIRCI) in critically ill patients (part I): Society of Critical Care Medicine (SCCM) and European Society of Intensive Care Medicine (ESICM) 2017. Intens. Care Med. 2017;43:1751-1763.
Pastores SM, Annane D, Rochwerg B. Corticosteroid Guideline Task Force of SCCM and ESICM. Guidelines for the diagnosis and management of critical illness-related corticosteroid insufficiency (CIRCI) in critically ill patients (part II): Society of Critical Care Medicine (SCCM) and European Society of Intensive Care Medicine (ESICM) 2017. Crit. Care Med. 2018;46:146-148.
Summers AM, Culler C, Yaxley PE, et al. Retrospective evaluation of the use of hydrocortisone for treatment of suspected critical illness-related corticosteroid insufficiency (CIRCI) in dogs with septic shock (2010-2017): 47 cases. J. Vet. Emerg. Crit. Care 2021;31:371-379.
Kenney EM, Rozanski EA, Rush JE, et al. Association between outcome and organ system dysfunction in dogs with sepsis: 114 cases (2003-2007). J. Am. Vet. Med. Assoc. 2010;236(1):83-87.
Rafael Obrador de Aguilar
Le Dr Obrador est diplômé de l’Université de Saragosse En savoir plus
Vous envisagez de faire un internat aux États-Unis ? Cet article présente brièvement les avantages et les inconvénients de ce type de projet.
Mettre en place une fluidothérapie chez un chat n’est pas aussi simple qu’il n’y paraît. Cet article fait la synthèse des connaissances actuelles à ce sujet.
L’insuffisance cardiaque aiguë chez un chien menace sérieusement son pronostic vital et Luca Ferasin explique ici combien il est important d’optimiser la démarche diagnostique et thérapeutique.
Que faites-vous lorsqu’un animal diabétique arrive à la clinique en urgence et dans un état critique ? Cet article propose d’optimiser la démarche grâce à une approche par étapes.
