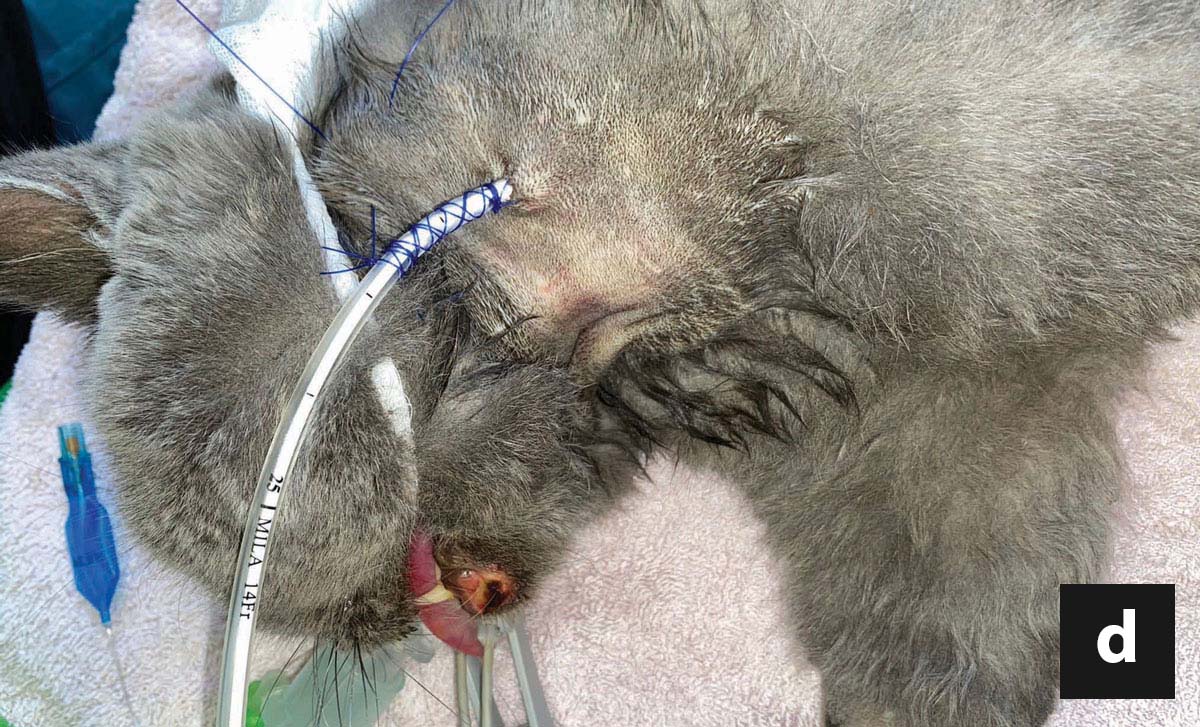
Les aliments de convalescence disponibles dans le commerce, riches en calories et en protéines, suffisent souvent à couvrir les besoins nutritionnels du chat en termes d’acides aminés et d’acides gras essentiels. Une restriction protéique est rarement indiquée, sauf en cas d’encéphalose hépatique sévère. L’apport calorique quotidien (besoin énergétique au repos = 30 x (poids corporel) + 70 ; ou (poids corporel)0,75 x70), sera réparti en 4 à 6 repas. Le volume de chaque repas, en incluant l’eau utilisée à la fin pour rincer la sonde d’alimentation, ne doit pas dépasser 10-15 mL/kg/repas. Il est en général conseillé d’augmenter progressivement le volume des repas et l’apport calorique global, sur une période de trois jours. Cela permet d’assurer une réadaptation progressive du tube digestif à l’alimentation, de surveiller le développement éventuel d’un iléus gastrique qui pourrait empêcher la poursuite de l’alimentation, et de réduire le risque d’un syndrome de réalimentation (voir le paragraphe « complications » ci-dessous).
Un déficit en vitamines liposolubles (par exemple : vitamine D, vitamine K) et hydrosolubles (par exemple : thiamine, cobalamine) apparaît chez les chats atteints de LHF 2. Comme ces carences sont associées à une foule de complications (notamment des coagulopathies, une atrophie villositaire, une hyperammoniémie, une anémie et des déficits neurologiques), la supplémentation en vitamines fait partie intégrante du traitement (Tableau 2).
Fluidothérapie et traitement antinauséeux
L’état d’hydratation, les besoins d’entretien et les pertes liquidiennes visibles (par exemple : vomissements/diarrhée) et invisibles seront pris en compte pour calculer les besoins quotidiens en liquide. L’éventualité d’une maladie cardiaque concomitante et la quantité d’eau administrée par voie entérale via la sonde d’alimentation doivent cependant également être considérées. Une supplémentation en potassium est souvent indiquée, sous forme de chlorure de potassium (KCl) ou de phosphate de potassium (KPO4) en cas d’hypophosphatémie concomitante (Tableau 2). Si le dosage du magnésium sanguin n’est pas réalisé, une approche conservatrice pourrait consister à compléter le soluté avec du sulfate de magnésium, à raison de 0,5 mEq/kg toutes les 24 heures pendant 2 jours.
Un traitement antinauséeux et antiémétique est conseillé dans tous les cas. Le métoclopramide, le maropitant et l’ondansétron sont utilisables selon différentes formes. La mirtazapine est souvent ajoutée en raison de ses effets antinauséeux et stimulant de l’appétit, en particulier chez les chats anorexiques après leur sortie de la clinique. Le métoclopramide présente l’avantage supplémentaire de favoriser la motilité gastrointestinale. Si un iléus se développe malgré le traitement au métoclopramide et la résolution de l’hypokaliémie, un traitement au cisapride (0,5 mg/kg toutes les 8 heures per os) doit être envisagé.
Traitement cytoprotecteur
Les lésions oxydatives et la baisse de la concentration en glutathion sont des complications connues de la LHF ; un traitement antioxydant est donc couramment prescrit aux chats affectés, notamment à base de SAMe et de silymarine. La SAMe est une molécule ubiquitaire impliquée dans de multiples mécanismes biochimiques 23,24, tandis que la silymarine (qui contient plusieurs composés dont la silibinine, l’ingrédient le plus abondant et le plus actif) exerce des effets anti-inflammatoires et cholérétique, en plus d’être un antioxydant 23. Plusieurs spécialités vétérinaires associent désormais la silymarine et la SAMe, mais si l’administration orale ou entérale n’est pas possible, la N-acétylcystéine peut être administrée par voie intraveineuse pour reconstituer la réserve hépatique en cystéine et contribuer à faire remonter le glutathion. Cette molécule ne présente cependant pas tous les avantages de la silymarine et de la SAMe, et elle peut provoquer des vomissements si elle est administrée trop rapidement 23. De la vitamine E pourrait aussi être utile car elle capte les radicaux libres et protège les phospholipides membranaires de l’oxydation ; ses effets secondaires sont minimes mais ses bénéfices cliniques n’ont pas été documentés 23 (Tableau 2).
Traitements divers
L’acide ursodésoxycholique, un acide biliaire hydrophile, pourrait s’avérer bénéfique au traitement de la LHF en raison de ses propriétés cholérétiques, anti-apoptotiques et anti-inflammatoires, et de la rareté de ses effets secondaires 23 (Tableau 2). La L-carnitine fait pénétrer les acides gras à longue chaîne dans les mitochondries, facilitant ainsi leur utilisation pour la production d’énergie ; chez les chats obèses soumis à une restriction alimentaire, elle limite l’accumulation de triglycérides hépatiques et les observations cliniques indiquent un effet bénéfique potentiel lors de LHF 10. Même si les chats atteints de LHF présentent une élévation du taux de carnitine 25, une carence relative peut subsister et une supplémentation est donc recommandée (Tableau 2). La carence en taurine est associée à diverses affections cardiaques, neurologiques, reproductives et développementales, et elle contribue à l’accumulation de lipides dans le foie. Les aliments du commerce contiennent des quantités adéquates de cet acide aminé mais une supplémentation entérale est parfois recommandée, en particulier si le chat reçoit de l’acide ursodésoxycholique, qui exacerbe la perte biliaire de taurine 1. Enfin, du lactulose peut être utile en cas de signes sévères d’encéphalose hépatique et d’hyperammoniémie, ou chez les chats constipés, tandis que le pantoprazole et l’oméprazole sont conseillés en présence d’une suspicion d’ulcère gastrique ou d’œsophagite par reflux.
Complications
De nombreuses complications peuvent apparaître à la suite d’une LHF et de son traitement. Le syndrome de réalimentation, dû au développement de multiples changements métaboliques suivant la reprise de l’alimentation après une période de malnutrition prolongée, est fréquemment mentionné mais peu documenté chez les chats. Il est associé à une hypophosphatémie sévère (parfois à une hypokaliémie), une hypomagnésémie et une carence en thiamine. L’augmentation progressive de l’apport calorique, la restriction glucidique, l’apport d’électrolytes à titre préventif et une surveillance étroite permettent d’éviter les conséquences délétères de ce syndrome 1,14,15.
Une atrophie villositaire diffuse est une autre complication susceptible d’apparaître en cas d’anorexie prolongée, entraînant une malabsorption et une diarrhée après réintroduction de l’alimentation entérale. La réalimentation progressive et l’utilisation d’aliments hautement digestibles limiteront alors le risque de diarrhée. Des affections concomitantes sont fréquentes chez les chats à LHF, notamment une pancréatite, des maladies rénales, des cardiomyopathies, des complications hémorragiques ou thrombotiques et une résistance à l’insuline. Des épanchements cavitaires peuvent également se développer à la suite d’une hypoalbuminémie, d’une maladie cardiaque ou d’une pancréatite, ce qui constitue un facteur de pronostic négatif 9.
Enfin, l’immunosuppression liée à la malnutrition prédispose à des infections bactériennes secondaires, et un traitement antibiotique sera indiqué si une infection est mise en évidence (une cholécystite par exemple). Dans certaines circonstances, un traitement antibactérien peut également être envisagé en cas de neutropénie ou neutrophilie sévère ou d’hypoglycémie, même si l’infection n’est pas prouvée par la cytologie ou la bactériologie.
Conclusion
La lipidose hépatique féline (LFH) est la maladie hépatique la plus fréquente chez les chats, et son pronostic dépend beaucoup de la présence éventuelle de maladies sous-jacentes et de comorbidités. Le taux de survie global varie entre 50 et 85 % mais la pancréatite aiguë, le ptyalisme, les épanchements cavitaires, l’hypoalbuminémie et un âge avancé au moment du déclenchement sont des exemples de marqueurs pronostiques négatifs. Néanmoins, bien que cette maladie soit associée à une morbidité importante, qu’elle nécessite un traitement intensif et qu’elle entraîne des dépenses importantes, le traitement est souvent couronné de succès et les récidives semblent rares.