Nematodi polmonari e filarie cardiopolmonari nei gatti
I nematodi polmonari e le filarie cardiopolmonari sono una minaccia sottovalutata ma potenzialmente grave per molti gatti, come rivela questo articolo.
Pubblicato il 13/10/2022
Disponibile anche in Français , Deutsch , Polski , Română , Español e English
La cardiomiopatia ipertrofica è prevalente nella popolazione di gatti di proprietà, ma non è sempre facile identificare gli animali colpiti; questo documento offre una panoramica completa della condizione per il medico veterinario di prima valutazione.

La cardiomiopatia ipertrofica (HCM) è la cardiomiopatia più diffusa nei gatti, ed è caratterizzata da ipertrofia ventricolare sinistra e funzione diastolica ridotta.
Il rilevamento di un soffio, un’aritmia, o un tono di galoppo nel gatto asintomatico richiede sempre ulteriori indagini cardiache.
L’ecocardiografia è lo strumento diagnostico standard di riferimento, poiché le dimensioni dell’atrio sinistro sono un indicatore prognostico importante.
L’HCM ha una progressione variabile e, spesso, una lunga fase preclinica; la stadiazione offre informazioni prognostiche e contribuisce a determinare la necessità di un trattamento o di variazioni nella gestione.
La cardiomiopatia ipertrofica felina (HCM) è una cardiomiopatia primaria definita in base all’ipertrofia concentrica del ventricolo sinistro (LV), cioè dall’ispessimento delle pareti di LV 1. È una malattia che comporta una disfunzione diastolica (compromissione del rilassamento), ma di norma la funzione sistolica (contrattilità) viene mantenuta. La ridotta compliance del miocardio compromette la capacità del cuore di rilassarsi e riempirsi durante la diastole, con conseguente aumento della pressione diastolica che esita in una dilatazione progressiva dell’atrio sinistro (LA) 2. L’HCM è una diagnosi per esclusione, ed è quindi indispensabile escludere le altre possibili malattie cardiache o sistemiche che possono causare o contribuire al fenotipo HCM, come ad esempio ipertensione sistemica, ipertiroidismo, acromegalia e stenosi aortica. La progressione della malattia è molto variabile e ha spesso una fase preclinica asintomatica prolungata che sfugge di frequente all’identificazione. I gatti possono presentare successivamente segni di insufficienza cardiaca congestizia (CHF), tromboembolia (TE) arteriosa o aritmie 2,3.
L’HCM è la cardiomiopatia felina più comune, e si stima colpisca il 14,5-34% della popolazione felina “sana” 1,4. I gatti Domestico a pelo corto e Domestico a pelo lungo rappresentano la maggior parte dei casi 4, ma le razze con pedigree e predisposizione per l’HCM includono Persiano, British Shorthair, Maine Coon, Ragdoll, Sphynx, Himalayano e Bengala. Qualsiasi età può essere colpita, ma i gatti di razza pura, in particolare, possono presentare la forma grave della malattia in giovane età 4. L’HCM è sovrarappresentata nei gatti maschi, rappresentando il 75% dei casi, nonostante non sia stato identificato alcun pattern ereditario legato al sesso.
Catheryn Partington
L’HCM familiare nei gatti Maine Coon, Ragdoll e Sphynx 5,6,7 è il risultato di mutazioni nelle proteine sarcomeriche, mentre in tutti gli altri gatti la causa rimane sconosciuta, sebbene sia probabilmente ereditabile in altri soggetti di razza pura. Il sarcomero è la componente contrattile dei cardiomiociti, e le mutazioni delle proteine sarcomeriche alterano la struttura e la funzione del sarcomero, finendo per compromettere le prestazioni del cardiomiocita. L’esatto processo con cui la disregolazione del sarcomero produce il fenotipo HCM è complesso e non completamente compreso. Le alterazioni nella sensibilità al calcio, nella funzione meccanica, e nello stress cellulare culminano nell’ipertrofia del miocita, nella sintesi di collagene, e nella degradazione del miocita, ovvero i tratti distintivi istopatologici dell’HCM felina 4,8.
Nel Maine Coon e nel Ragdoll sono state identificate due diverse mutazioni (rispettivamente A31P e R820W) della proteina C legante la miosina nel sarcomero 5,6. I soggetti eterozigoti per la mutazione hanno spesso la malattia subclinica, con alterazioni solo a livello cellulare, non macroscopico; i gatti omozigoti, invece, sono colpiti più gravemente; si sospetta una modalità ereditaria di dominanza incompleta. I Maine Coon privi della mutazione possono ancora sviluppare un fenotipo HCM, riflettendo così la probabile eziologia multifattoriale della condizione. Più di recente è stata identificata una mutazione nel gene ALMS1* come fattore causale dell’HCM nei gatti Sphynx 7.
* ALMS1 = sindrome di Alstrom 1
Come indicato sopra, l’HCM si manifesta come ipertrofia del LV e disfunzione diastolica, motivo per cui le alterazioni patologiche riducono la capacità del ventricolo di rilassarsi e riempirsi durante la diastole. Inoltre, l’ipertrofia parietale progressiva riduce l’apporto ematico ai cardiomiociti, che vengono sostituiti da tessuto fibroso alla loro morte, riducendo ulteriormente la compliance miocardica (cioè, maggiore rigidità). Di conseguenza, per ogni dato volume di sangue aumenta la pressione diastolica nel LV, innalzando a sua volta la pressione nel LA che poi si dilata. La pressione elevata del LA viene rimandata indietro alle vene polmonari, e quando la pressione venosa polmonare supera i 25 mmHg, si ha edema polmonare, l’aspetto caratteristico della CHF sinistra 4. Nei gatti, le vene che drenano la pleura polmonare si aprono nelle vene polmonari, consentendo lo sviluppo del versamento pleurico con CHF sinistra (a differenza dei cani, dove il versamento pleurico è sempre il risultato della CHF destra, mai di quella sinistra) 4.
La dilatazione progressiva del LA è uno dei fattori che predispongono i gatti con HCM grave alla malattia tromboembolica, anche se questa condizione esula dallo scopo di questo articolo. L’ipertrofia marcata, l’apporto ridotto di ossigeno, e la fibrosi sostitutiva nel miocardio agiscono da substrati per lo sviluppo delle aritmie.
L’ipertrofia del LV nell’HCM felina può interessare il setto interventricolare e anche la parete libera; in alternativa, le alterazioni possono essere asimmetriche, con appena una regione focale interessata, generalmente la base del setto interventricolare. L’ipertrofia può interessare anche il ventricolo destro, ma il pattern e la distribuzione possono essere molto variabili tra un soggetto e l’altro (Figure 1 e 2) 4. Potrebbero esserci anche alterazioni nell’apparato della valvola mitrale, inclusi l’allungamento del lembo anteriore della valvola mitrale e l’ipertrofia del muscolo papillare. Il movimento anteriore sistolico (SAM) della valvola mitrale è una caratteristica comune dell’HCM e può causare una significativa ostruzione del tratto di efflusso ventricolare sinistro (LVOTO) 9,10.


Figura 1. Il pattern di ipertrofia del LV nella cardiomiopatia ipertrofica felina può essere molto variabile tra un soggetto e l’altro, ma questi campioni anatomopatologici mostrano un’ipertrofia ventricolare sinistra diffusa.
Abbreviazioni: LVFW, parete libera ventricolare sinistra; IVS, setto interventricolare; RV, ventricolo destro
Per gentile concessione di Emanuele Ricci, University of Liverpool Regno Unito

Figura 2a. Le viste ecocardiografiche dell’HCM possono mostrare una grande variabilità. (a) Vista a 5 camere in asse lungo parasternale destro, che mostra una regione di ipertrofia focale che interessa il setto basale (*).
Credit: Catheryn Partington – Joanna Dukes-McEwan

Figura 2b. Le viste ecocardiografiche dell’HCM possono mostrare una grande variabilità. Vista in asse corto parasternale destro a livello dei muscoli papillari, che mostra ipertrofia ventricolare sinistra e del muscolo papillare.
Credit: Catheryn Partington – Joanna Dukes-McEwan

Figura 2c. Le viste ecocardiografiche dell’HCM possono mostrare una grande variabilità. Vista a 4 camere in asse lungo parasternale destro, che mostra ipertrofia simmetrica del setto interventricolare e della parete libera ventricolare sinistra.
Credit: Catheryn Partington – Joanna Dukes-McEwan
Abbreviazioni: LA, atrio sinistro; LV, ventricolo sinistro; Pm, muscolo papillare.
Un sottogruppo di gatti con HCM può avere una LVOTO significativa (Figura 3). Tali casi sono stati classicamente definiti cardiomiopatia ostruttiva ipertrofica (HOCM), ma la medicina umana ha abbandonato questo termine poiché la presenza della LVOTO può essere intermittente; inoltre, dato che questo vale anche per i gatti, il termine è probabilmente obsoleto 3,9,11. La LVOTO può essere il risultato di SAM della valvola mitrale, ipertrofia focale del setto basale o, meno spesso, ostruzione della cavità media dovuta all’ipertrofia del muscolo papillare 4,9,12. Questa LVOTO provoca un soffio dovuto all’aumento della turbolenza del sangue. Con il SAM, l’ostruzione è generalmente dinamica, e peggiora all’aumento della contrattilità cardiaca, come ad esempio durante uno stress fisico o emotivo. Questo è spesso il motivo della presenza o intensità variabile dei soffi nei gatti con HCM.
Il SAM della valvola mitrale avviene quando il lembo settale (anteriore) (spesso allungato) viene tirato verso il tratto di efflusso a causa dell’ipertrofia e dislocazione del muscolo papillare, con conseguente allentamento delle corde tendinee 10. Quando il tratto di efflusso si restringe a causa di questo movimento anomalo del lembo (o dell’ipertrofia settale basale), la velocità del sangue aumenta e la pressione diminuisce, trascinando ulteriormente la punta del lembo nel tratto di efflusso e peggiorando l’ostruzione (effetto Venturi) 4,9. Si ritiene che il SAM aumenti la richiesta di ossigeno del miocardio e riduca la perfusione coronarica, aumentando così il rischio di ischemia miocardica; questo è probabilmente associato all’ipertrofia e alla disfunzione microvascolare progressive. Si ritiene che alcuni gatti con LVOTO grave mostrino segni di capacità ridotta all’esercizio fisico e dolore di tipo anginoso, come descritto nell’uomo.

Figura 3a. I soffi nei gatti con HCM derivano molto spesso dall’ostruzione del tratto di efflusso ventricolare sinistro (LVOTO). Vista a 5 camere in asse lungo parasternale destro con Doppler flusso di colore che mostra un getto turbolento del flusso ematico nel tratto di efflusso ventricolare sinistro (freccia aperta) causato dal movimento anteriore sistolico della valvola mitrale, e un piccolo getto eccentrico di rigurgito mitralico (freccia piccola).
Credit: Catheryn Partington – Joanna Dukes-McEwan

Figura 3b. I soffi nei gatti con HCM derivano molto spesso dall’ostruzione del tratto di efflusso ventricolare sinistro (LVOTO). Vista a 5 camere in asse lungo parasternale destro che mostra ipertrofia settale basale focale (*) come causa di LVOTO.
Credit: Catheryn Partington – Joanna Dukes-McEwan

Figura 3c. I soffi nei gatti con HCM derivano molto spesso dall’ostruzione del tratto di efflusso ventricolare sinistro (LVOTO). Doppler spettrale del LVOT che mostra velocità aumentate (*) e accelerazione bifasica (classica forma a “scimitarra”), indicative di LVOTO.
Per gentile concessione di J. Novo Matos, University of Cambridge, Regno Unito.
Abbreviazioni: Ao, aorta; LA, atrio sinistro; LV, ventricolo sinistro
L’ispessimento miocardico transitorio (TMT) è una diagnosi differenziale importante per un fenotipo HCM. È raro e poco compreso, ma è caratterizzato da aumenti nello spessore parietale del LV e nella dilatazione del LA che sono meno marcati di quelli osservati nell’HCM primaria; inoltre, è caratterizzato dalla piena risoluzione dei segni clinici e delle alterazioni ecocardiografiche nell’arco di alcuni mesi. Il TMT è quindi associato a una prognosi eccellente. I gatti con CHF secondaria a TMT tendono a essere più giovani di quelli con HCM primaria, e viene spesso segnalato un evento antecedente (come ad esempio l’anestesia generale). È stato ipotizzato che l’aumento dello spessore parietale sia dovuto all’edema miocardico, mostrando analogie sia con la miocardite acuta, sia con la cardiomiopatia da stress nell’uomo 13.
Le recenti linee guida ACVIM sulla diagnosi e il trattamento dell’HCM 14 descrivono un sistema di stadiazione simile a quello utilizzato per la valvulopatia mitralica mixomatosa nei cani (Riquadro 1). Questo sistema può aiutare a determinare se il trattamento è indicato, oltre a fornire ai proprietari alcune previsioni sull’evoluzione futura, poiché la progressione dell’HCM, e quindi la prognosi, è fortemente variabile. In alcuni gatti, la malattia è progressiva, esitando in CHF, TE e morte cardiaca, mentre altri possono rimanere preclinici e morire infine per cause non cardiache 14,15. La ragione di tale caratteristica di eterogenesi rimane poco chiara, ed è difficile prevedere quali gatti possano morire come conseguenza della malattia, sebbene molti studi retrospettivi abbiano identificato una serie di fattori prognostici. I gatti con diagnosi in giovane età tendono ad avere tempi di sopravvivenza più lunghi 2. I gatti che sviluppano una CHF secondaria a fattori come ad esempio lo stress o la fluidoterapia endovenosa (IVFT) hanno generalmente una sopravvivenza più lunga rispetto ad altri gatti con HCM in Stadio C. La presenza di toni di galoppo, aritmie, grave dilatazione del LA, funzione sistolica del LA ridotta, contrasto eco spontaneo, ipertrofia parietale grave (>9 mm), disfunzione sistolica del LV e assottigliamento parietale focale è associata a un rischio aumentato di CHF e/o di TE 2,15.
Riquadro 1. Stadiazione ACVIM dell’HCM felina.
 |
Stadio A |
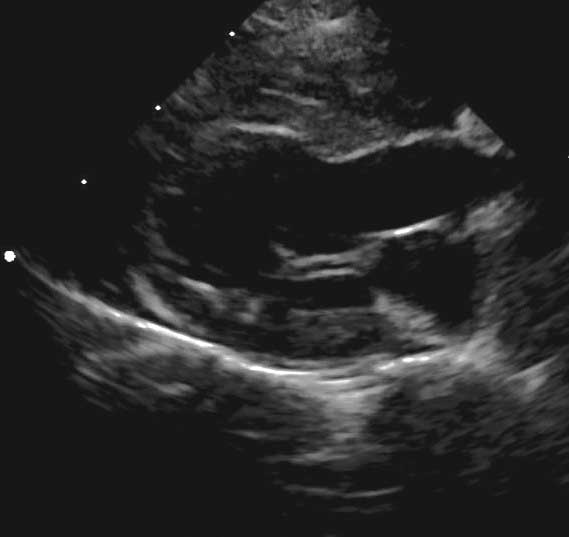
Stadio A: gatti predisposti all’HCM, ma senza evidenza attuale; ad es. un Maine Coon con mutazione genetica A31P, o un gatto che ha un parente stretto con diagnosi di HCM. Il cuore appare strutturalmente normale alla scansione ecografica. |
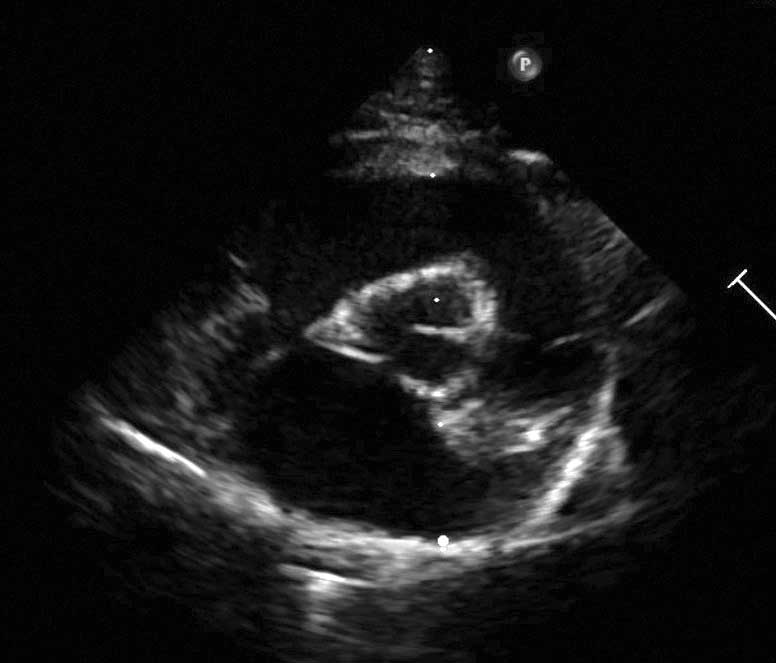 |
Stadio B1 |
Stadio B: gatti con HCM preclinica (cioè, assenza di segni clinici ma evidenza ecocardiografica di HCM). Questo stadio è ulteriormente suddiviso in base alla gravità della malattia e al rischio di CHF e TE.
|
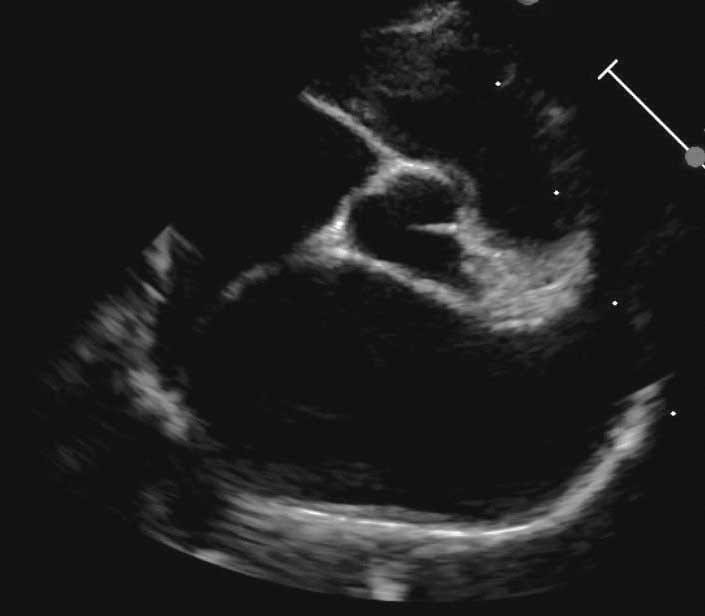 |
Stadio B2 | |
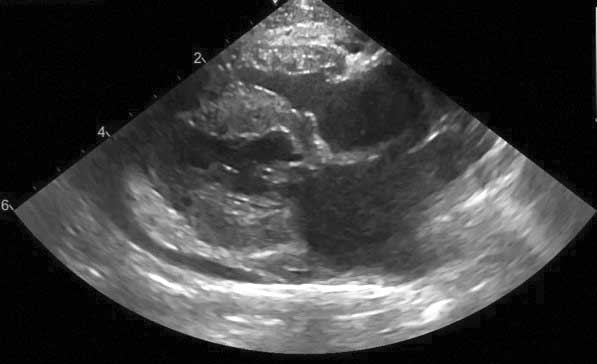 |
Stadio C | Stadio C: gatti con segni clinici di HCM e CHF o TE. |
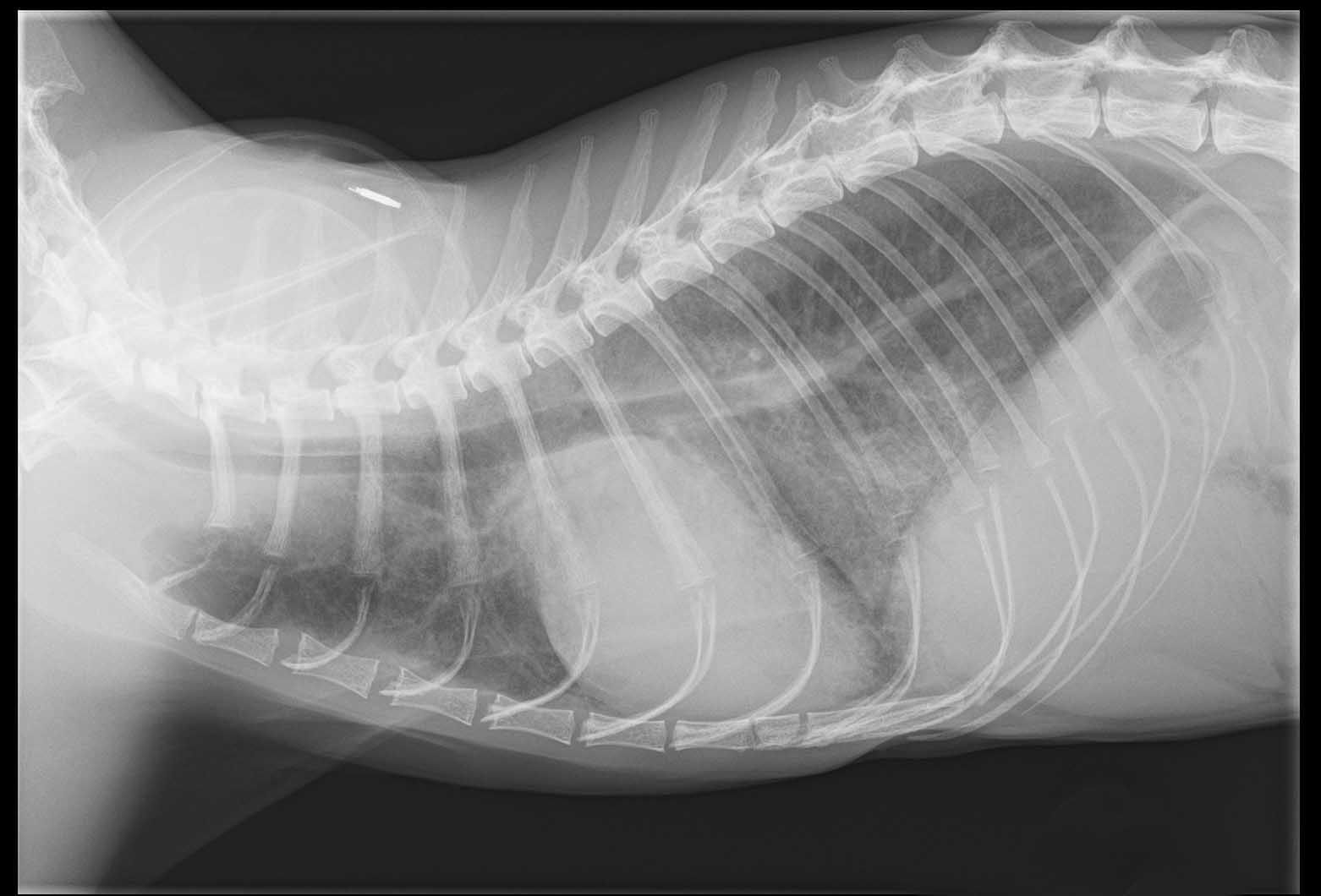 |
Stadio D | Stadio D: gatti con HCM e CHF refrattari al trattamento. |
Credit: Catheryn Partington
Data la funzione diastolica ridotta e il conseguente aumento delle pressioni per ogni dato volume di sangue nel LV, i gatti con HCM sono più sensibili agli aumenti del volume circolante (cioè, all’aumento del precarico). Alcuni trattamenti, come ad esempio uso di corticosteroidi prolungato e IVFT, potrebbero quindi portare un gatto con HCM avanzata a sviluppare CHF sinistra. Ciò evidenzia l’importanza di identificare i gatti con malattia preclinica, in modo da poter modificare e monitorare strettamente tali trattamenti (ad es. velocità di IVFT più basse, monitoraggio più attento delle frequenze respiratorie, e imaging sequenziale per valutare le dimensioni dell’atrio sinistro) al fine di ridurre il rischio di scompenso. Inoltre, i gatti con HCM avanzata sono a rischio di tromboembolia, e la loro identificazione consente di avviare una terapia antipiastrinica preventiva.
L’identificazione dei gatti in Stadio B può facilitare l’individuazione dei segni deboli di progressione precoce allo Stadio C, poiché i proprietari possono essere più informati e vigili per quanto riguarda i segni di CHF, consentendo così l’avvio del trattamento prima di arrivare all’edema polmonare fulminante e alla compromissione respiratoria grave.
La sfida nell’HCM risiede nella durata variabile della fase preclinica, assieme alla frequente assenza di segni clinici o alterazioni all’esame obiettivo. Le alterazioni alla visita clinica che potrebbero far sorgere il sospetto di HCM in Stadio B includono la presenza di un soffio (Riquadro 2), toni di galoppo (Riquadro 3) o aritmia 4. Sebbene molti gatti asintomatici con HCM abbiano un soffio, oltre il 31-62% non avrà tale disturbo; inoltre, il 25-33% dei gatti con soffi sistolici parasternali a sinistra (generalmente deboli, di basso grado) non ha un’evidenza ecocardiografica di cardiomiopatia 1,4. È più probabile che i soffi più forti (> grado 3/6) siano associati a una cardiopatia significativa 4, ma qualsiasi soffio giustifica ulteriori indagini.
Riquadro 2. Cause dei soffi nell’HCM preclinica.
|
Quando il flusso ematico diventa turbolento si percepiscono soffi; ciò può essere dovuto a flusso ematico molto rapido, vasi di grande diametro, alta densità del fluido o bassa viscosità. Nell’HCM, i soffi derivano quasi sempre dall’ostruzione del tratto di efflusso ventricolare sinistro (LVOT) dovuta al movimento anteriore sistolico della valvola mitrale e/o all’ipertrofia settale basale focale.
I soffi nei gatti con HCM sono spesso dinamici, cioè possono cambiare di intensità ed essere anche talvolta assenti. Il grado di ostruzione è probabilmente peggiore quando il cuore si contrae con maggior forza (cioè, quando aumentano le catecolamine a causa dello stress), creando un soffio più forte.
|
Riquadro 3. Cosa sono i toni di galoppo?
|
Nella maggior parte dei cani e gatti sani, l’auscultazione consente di rilevare solo il primo (S1) e il secondo (S2) dei toni cardiaci. Il tono di galoppo è un ulteriore tono cardiaco udibile che crea una cadenza di tre battiti, simile ai passi di un cavallo al galoppo. Ciò può essere dovuto a un terzo (S3) o un quarto (S4) tono cardiaco udibile, sebbene sia spesso difficile distinguere tali toni all’auscultazione. S3 deriva dal riempimento ventricolare rapido in diastole precoce, mentre S4 è il risultato del riempimento ventricolare attivo tramite la contrazione atriale in telediastole.
L’auscultazione di toni di galoppo è generalmente indicativa della presenza di una disfunzione diastolica, e il 2,6-19% dei gatti con HCM subclinica ha un tono di galoppo 19. Vengono raramente percepiti all’auscultazione nei gatti sani, quindi la loro identificazione giustifica sempre ulteriori indagini cardiache.
|
Credit: Catheryn Partington – Joanna Dukes-McEwan
L’ecocardiografia è lo standard di riferimento per la diagnosi di HCM 14, e se viene identificata un’ipertrofia, è raccomandabile indagare le cause dell’ipertrofia secondaria. L’ecocardiografia va consigliata per tutti i gatti con segni clinici possibilmente attribuibili a una cardiomiopatia (sincope, intolleranza all’esercizio fisico, intolleranza all’IVFT), per i soggetti con anamnesi familiare di HCM (o morte improvvisa), per i gatti con pedigree destinati alla riproduzione, e per i gatti dove i riscontri dell’esame obiettivo sono indicativi di una cardiomiopatia (toni di galoppo, aritmie, soffio, tachipnea, dispnea, suoni polmonari ridotti). La dichiarazione di consenso di ACVIM ha inoltre consigliato di effettuare una valutazione ecocardiografica nei gatti di età superiore ai 9 anni da sottoporre a interventi che possono precipitare la CHF (ad es. anestesia generale, IVFT e terapia corticosteroidea prolungata) 14.
Per il gatto asintomatico, l’ecocardiografia consente di valutare quattro criteri principali: spessore parietale del LV, dimensioni del LA, presenza di LVOTO, e funzione diastolica. Nei casi di malattia moderata-grave, i primi due criteri possono essere valutabili in modo relativamente semplice da un medico veterinario generalista con competenze ecografiche di base.
1. Spessore parietale ventricolare sinistro
Si raccomanda di valutare sia il setto interventricolare che la parete libera del LV, ed effettuare le misurazioni mediante ecocardiografia 2D, sulle proiezioni parasternali di destra alla telediastole (il fotogramma precedente la chiusura dei lembi della valvola mitrale) (Figura 4a). Dato che l’ipertrofia può essere focale, le misurazioni vanno effettuate su almeno tre cicli cardiaci e, idealmente, da posizioni multiple. Nelle misurazioni della parete è indispensabile prestare attenzione a non includere i muscoli papillari o le regioni con ispessimento endocardico marcato. Uno spessore parietale del LV in telediastole inferiore a 5 mm è normale, mentre ≥6 mm è compatibile con l’ipertrofia 14. I valori pari a 5-6 mm rimangono un’area grigia e vanno considerati rispetto alla taglia corporea, alla razza, e ad altre variabili ecocardiografiche 16.

Figura 4a. Valutazione ecocardiografica della cardiomiopatia ipertrofica (HCM). Vista a 5 camere in asse lungo parasternale destro. Lo spessore della parete libera ventricolare sinistra e del setto interventricolare va misurato su immagini 2D in diastole; valori ≥6 mm sono compatibili con l’ipertrofia.
Credit: Catheryn Partington – Joanna Dukes-McEwan
2. Dimensione atriale sinistra
Le dimensioni del LA sono un fattore di rischio indipendente per CHF, TE e morte cardiaca, e possono essere valutate alle proiezioni parasternali di destra, sia in asse lungo che in asse corto. Nelle proiezioni in asse corto a livello della base del cuore, le misurazioni vengono effettuate in diastole precoce (il fotogramma seguente la chiusura delle cuspidi della valvola aortica), con il diametro atriale indicizzato all’aorta (LA/Ao; Figura 4b). L’aorta viene misurata dal punto medio della curvatura convessa della parete del seno aortico destro, al punto in cui si fondono la parete aortica, le cuspidi aortiche non coronariche, e le cuspidi aortiche coronariche di sinistra. L’LA viene misurato da quest’ultimo punto alla parete libera del LA, evitando di entrare nella vena polmonare 17.

Figura 4b. Valutazione ecocardiografica della cardiomiopatia ipertrofica (HCM). Vista in asse corto parasternale destro a livello della base del cuore. Le dimensioni dell’atrio sinistro sono indicizzate alla radice aortica (LA/Ao), e misurate in diastole precoce; valori >1,6 sono compatibili con la dilatazione atriale sinistra.
Credit: Catheryn Partington – Joanna Dukes-McEwan
Sulla proiezione a quattro camere in asse lungo parasternale destro, l’LA dovrebbe essere ottimizzato e il diametro atriale sinistro (LAD) misurato alla telesistole (il fotogramma precedente l’apertura del lembo della valvola mitrale), tracciando una linea parallela all’anello mitralico che va dal setto interatriale alla parete libera del LA (Figura 4c) 18. Valori di LA/Ao >1,6 e LAD >16,0 mm sono compatibili con la dilatazione del LA; valori di LA/Ao >1,8-2,0 o LAD >18-19 mm sono considerati una dilatazione del LA moderata-grave. Per valutare la funzione sistolica è inoltre possibile determinare la frazione di accorciamento del LA. Nella valutazione del rischio di CHF e TE sono anche importanti la valutazione soggettiva delle dimensioni dell’auricola sinistra, la presenza di contrasto eco spontaneo o di un trombo, e la valutazione delle velocità dell’auricola sinistra.

Figura 4c. Valutazione ecocardiografica della cardiomiopatia ipertrofica (HCM). Vista a 4 camere in asse lungo parasternale destro. Il diametro dell’atrio sinistro viene misurato parallelamente all’anello mitralico alla telesistole; valori >16,0 mm sono compatibili con la dilatazione atriale sinistra.
Credit: Catheryn Partington – Joanna Dukes-McEwan
Abbreviazioni: Ao, aorta; IVS, setto interventricolare; LA, atrio sinistro; LV, ventricolo sinistro; LVFW, parete libera ventricolare sinistra; MV, valvola mitrale.
3. Presenza di ostruzione del LVOT
Questa può essere valutata nelle modalità Doppler 2D, M-mode, flusso di colore, e spettrale (Figura 3c). Il SAM può essere visualizzato sia in modalità 2D che in M-mode. La modalità Doppler flusso di colore evidenzia la turbolenza nel LVOT e possibilmente il rigurgito mitralico. La modalità Doppler spettrale per valutare le velocità del LVOT richiede un valido allineamento al flusso; con l’ostruzione dinamica, il profilo Doppler mostra spesso un’accelerazione bifasica (classica forma a scimitarra).
4. Funzione diastolica
La funzione diastolica può essere valutata sia dal Doppler spettrale che dall’imaging Doppler tissutale, ma l’ulteriore discussione esula dallo scopo di questo articolo. I gatti con HCM avanzata possono anche avere una compromissione della funzione sistolica.
La radiografia toracica è lo standard di riferimento per la diagnosi di edema polmonare, ma è meno utile nei gatti asintomatici 14. Si può osservare una grave cardiomegalia con rigonfiamento del LA, e tuttavia le radiografie hanno una sensibilità inferiore nell’identificazione del rimodellamento lieve-moderato nei pazienti con HCM, molti dei quali possono avere una silhouette cardiaca normale.
I biomarcatori saranno discussi più dettagliatamente in altre sedi ma, senza scendere nei dettagli, possono essere uno strumento utile se usati in aggiunta ad altri strumenti diagnostici e per monitorare la progressione della malattia, anche se vanno impiegati con cautela come strumento di screening. Per il gatto asintomatico, l’NT-proBNP quantitativo (un marcatore di stress e allungamento miocardico) ha un uso limitato come strumento di screening nella popolazione generale; infatti, sebbene abbia un’elevata specificità, la sensibilità è bassa, il che significa rischio elevato di dare risultati falsi negativi. Il test è probabilmente migliore se utilizzato selettivamente nei casi di sospetta cardiomiopatia (cioè, quando si rileva un soffio) 19, e insieme all’ecocardiografia per comprendere meglio la gravità della cardiomiopatia. L’analisi decentrata (da banco) dell’NT-proBNP è più utile nel gatto sintomatico per differenziare le cause di dispnea cardiache e non cardiache 20.
La troponina cardiaca I (Tn I), un marcatore di lesione del cardiomiocita, è utile ancora una volta insieme all’ecocardiografia, e ha dimostrato una significatività prognostica, con i valori aumentati associati agli esiti peggiori 21. L’ischemia miocardica può produrre livelli elevati, come segnalato nell’HCM felina avanzata. Forti aumenti possono far sorgere il sospetto di una miocardite che produce un fenotipo HCM secondario, giustificando ulteriori indagini.
Entrambi i biomarcatori hanno dimostrato di essere aumentati nei gatti con HCM e SAM, rispetto a quelli con HCM senza SAM, e persino nei gatti con dimensioni del LA normali/ambigue 22.
Test genetici sono disponibili per i gatti Maine Coon, Ragdoll e Sphynx (Figura 5), e sono raccomandati in tutti i gatti da riproduzione di queste razze, al fine di ridurre la prevalenza ereditaria di HCM. Si consiglia di non destinare alla riproduzione i soggetti omozigoti per la mutazione, mentre gli eterozigoti possono essere accoppiati con i soggetti negativi per la mutazione 14. È tuttavia importante che gli allevatori siano consapevoli del fatto che anche i gatti senza mutazioni genetiche conosciute possono sviluppare HCM.

Figura 5. I medici veterinari di una struttura di prima valutazione devono prestare attenzione ai segni di HCM nei loro pazienti, e tutte le visite di soggetti felini dovrebbero includere un’auscultazione cardiaca accurata alla ricerca di soffi, toni di galoppo e aritmie, ognuno dei quali giustifica ulteriori indagini. Questo vale in particular modo nelle razze soggette al cardiomiopatie, e oggi sono disponibili test per rilevare la mutazione genetica potenzialmente responsabile dell’HCM nel gatto Sphynx.
Credit: Shutterstock
La stadiazione dei gatti con HCM può aiutare a standardizzare il trattamento. Per i gatti in Stadio A e B1 (dilatazione atriale sinistra assente/minima) non è indicato alcun trattamento, salvo i casi di LVOTO grave, in cui possono essere considerati i betabloccanti (vedere di seguito). I gatti in Stadio B2 sono a rischio di TE ed è consigliato il clopidogrel come terapia preventiva.
Come nel caso dell’HCM umana, nella fisiopatologia dell’HCM felina è stato dimostrato il probabile coinvolgimento dell’insulina, del fattore di crescita insulinosimile 1, e dell’infiammazione. Le modifiche della dieta che puntano a questi fattori possono quindi avere effetti benefici; uno studio ha dimostrato che i gatti con HCM preclinica che ricevevano una dieta a basso contenuto di amido e integrata con acidi grassi omega-3 avevano un rimodellamento del LV ridotto. Qualora tali diete cardiache diventassero commercialmente disponibili in futuro, potrebbero essere considerate un intervento terapeutico nei gatti in Stadio B 23.
Nei pazienti umani con HCM e LVOTO grave, sono spesso segnalate intolleranza all’esercizio fisico e angina, con i segni clinici che migliorano dopo la terapia con betabloccanti. Il loro uso nei gatti preclinici con evidenza di LVOTO rimane discutibile, e le autrici consigliano pertanto di inviare i casi a un cardiologo per assistenza nella decisione. Teoricamente, i betabloccanti sembrerebbero favorevoli nei casi di LVOTO marcata; gli effetti inotropi e cronotropi negativi possono ridurre la gravità dell’ostruzione, migliorando al tempo stesso l’apporto di ossigeno al miocardio, e riducendo il rischio di aritmie e ischemia. Tuttavia, non è stato dimostrato alcun beneficio per la sopravvivenza a lungo termine, né per la qualità di vita 24,25. Inoltre, i betabloccanti sono controindicati nei casi di CHF, e sarebbero probabilmente dannosi per i gatti vicini allo scompenso.
Joanna Dukes-McEwan
Dato che l’HCM ha una prevalenza elevata nei gatti, con una tendenza per una fase preclinica lunga, e un rischio di segni clinici gravi, il medico veterinario generalista deve prestare attenzione ai segni della malattia in Stadio B nei propri pazienti felini. Tutti gli esami dovrebbero includere un’auscultazione accurata alla ricerca di soffi, toni di galoppo e aritmie, ognuno dei quali giustificherebbe ulteriori indagini. Il rilevamento di gatti in Stadio B consente l’avvio della terapia preventiva, ove applicabile, nonché la gestione del rischio prima di interventi o trattamenti che potrebbero far precipitare lo scompenso. Migliorare la formazione e la vigilanza del proprietario può anche facilitare l’identificazione dell’insufficienza cardiaca congestizia, prima che si sviluppi una compromissione respiratoria grave.
Payne JR, Brodbelt DC, Luis Fuentes V. Cardiomyopathy prevalence in 780 apparently healthy cats in rehoming centres (the CatScan study). J. Vet. Cardiol. 2015;17 Suppl 1:S244-S257.
Fox PR, Keene BW, Lamb K, et al. International collaborative study to assess cardiovascular risk and evaluate long-term health in cats with preclinical hypertrophic cardiomyopathy and apparently healthy cats: the REVEAL study. J. Vet. Intern. Med. 2018;32:930-943.
Kittleson MD, Cote E. The feline cardiomyopathies: 2. Hypertrophic Cardiomyopathy. J. Feline Med. Surg. 2021;23:1028-1051.
Cote E, MacDonald KA, Meurs KM, et al. Hypertrophic Cardiomyopathy. In: Feline Cardiology. 1st ed. John Wiley & Sons, Inc. 2011 Chapter 11;101-175.
Meurs KM, Sanchez X, David RM, et al. A cardiac myosin binding protein C mutation in the Maine Coon cat with familial hypertrophic cardiomyopathy. Hum. Mol. Genet. 2005;14:3587-3593.
Meurs KM, Norgard MM, Ederer MM, et al. A substitution mutation in the myosin binding protein C gene in Ragdoll hypertrophic cardiomyopathy. Genomics 2007;90:261-264.
Meurs KM, Williams BG, de Prospero D, et al. A deleterious mutation in the ALMS1 gene in a naturally occurring model of hypertrophic cardiomyopathy in the Sphynx cat. Orphanet J. Rare Dis. 2021;16:108.
Kittleson MD, Meurs KM, Harris SP. The genetic basis of hypertrophic cardiomyopathy in cats and humans. J. Vet. Cardiol. 2015;17 Suppl 1:S53-S73.
Schober K, Todd A. Echocardiographic assessment of left ventricular geometry and the mitral valve apparatus in cats with hypertrophic cardiomyopathy. J. Vet. Cardiol. 2010;12:1e16.
Seo J, Novo Matos J, Payne JR, et al. Anterior mitral valve leaflet length in cats with hypertrophic cardiomyopathy. J. Vet. Cardiol. 2021;37:62-70.
Maron BJ, Maron MS. A discussion of contemporary nomenclature, diagnosis, imaging, and management of patients with hypertrophic cardiomyopathy. Am. J. Cardiol. 2016;118:1897-1907.
MacLea HB, Boon JA, Bright JM. Doppler echocardiographic evaluation of mid ventricular obstruction in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2013;27:1416-1420.
Novo Matos J, Pereira N, Glaus T, et al. Transient myocardial thickening in cats associated with heart failure. J. Vet. Intern. Med. 2018;32(1):48-56.
Luis Fuentes V, Abbott J, Chetboul V, et al. ACVIM consensus statement guidelines for the classification, diagnosis, and management of cardiomyopathies in cats. J. Vet. Intern. Med. 2020;34:1062-1077.
Payne JR, Borgeat K, Connolly DJ, et al. Prognostic indicators in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2013;27:1427-1436.
Haggstrom J, Andersson AO, Falk T, et al. Effect of body weight on echocardiographic measurements in 19,866 pure-bred cats with or without heart disease. J. Vet. Intern. Med. 2016;30:1601-1611.
Hansson K, Haggstrom J, Kvart C, et al. Left atrial to aortic root indices using two-dimensional and M-mode echocardiography in Cavalier King Charles Spaniels with and without left atrial enlargement. Vet. Radiol. Ultrasound 2002;43(6):569-575.
Linney CJ, Dukes-McEwan J, Stephenson HM, et al. Left atrial size, atrial function and left ventricular diastolic function in cats with hypertrophic cardiomyopathy. J. Small. Anim. Pract. 2014;55(4):198-206.
Fox PR, Rush JE, Reynolds CA, et al. Multicenter evaluation of plasma N-terminal probrain natriuretic peptide (NT-pro BNP) as a biochemical screening test for asymptomatic (occult) cardiomyopathy in cats. J. Vet. Intern. Med. 2011;25:1010-1016.
Ward JL, Lisciandro GR, Ware WA, et al. Evaluation of point-of-care thoracic ultrasound and NT-proBNP for the diagnosis of congestive heart failure in cats with respiratory distress. J. Vet. Intern. Med. 2018;32:1530-1540.
Borgeat K, Sherwood K, Payne J, et al. Plasma cardiac troponin I concentration and cardiac death in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2014;28:1731-1737.
Seo J, Payne JR, Novo Matos J, et al. Biomarker changes with systolic anterior motion of the mitral valve in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2020;34(5):1718-1727.
van Hoek I, Hodgkiss-Geere H, Bode EF, et al. Association of diet with left ventricular wall thickness, troponin I and IGF-1 in cats with subclinical hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2020;34(6):2197-2210.
Schober KE, Zientek J, Li X, et al. Effect of treatment with atenolol on 5-year survival in cats with preclinical (asymptomatic) hypertrophic cardiomyopathy. J. Vet. Cardiol. 2013;15:93-104.
Coleman AE, DeFrancesco TC, Griffiths EH, et al. Atenolol in cats with subclinical hypertrophic cardiomyopathy: a double-blind, placebo-controlled, randomized clinical trial of effect on quality of life, activity, and cardiac biomarkers. J. Vet. Cardiol. 2020;30:77-91.
Catheryn Partington
La Dr.ssa Partington ha conseguito la laurea all’University of Liverpool nel 2014, conseguendo anche un Master in Veterinary Science, quindi è tornata nell’università per un internato a rotazione e una residenza in cardiologia, completando quest’ultima nel 2021 Scopri di più
Joanna Dukes-McEwan
La Professoressa Dukes-McEwan ha conseguito la laurea nel 1986 all’University of Glasgow dove è rimasta per svolgere un internato e un corso di formazione residenziale Scopri di più
I nematodi polmonari e le filarie cardiopolmonari sono una minaccia sottovalutata ma potenzialmente grave per molti gatti, come rivela questo articolo.
L’ernia diaframmatica è una conseguenza comune della lesione traumatica nei gatti e può essere fatale se non viene diagnosticata e trattata tempestivamente; questo articolo analizza la fisiopatologia e il trattamento della condizione.
Il chilotorace è una diagnosi differenziale per qualsiasi gatto con versamento pleurico, e in questo articolo Elizabeth Rozanski descrive l’approccio preferito in questi casi.
L’asma è una malattia comune nei gatti, ma può simulare molte altre patologie complicando di molto la diagnosi e il trattamento della condizione, come spiega questo articolo.
