Lungenwürmer und Herzwürmer bei Katzen
Lungenwürmer und Herzwürmer sind eine unterschätzte, aber potenziell ernste Bedrohung für viele Katzen, wie uns dieser Artikel erläutert.
Ausgabe nummer 32.2 Kardiologie
veröffentlicht 13/10/2022
Auch verfügbar auf Français , Italiano , Polski , Română , Español und English
Die hypertrophe Kardiomyopathie kommt in der Katzenpopulation häufig vor, betroffene Tiere sind aber nicht einfach zu erkennen. Dieser Artikel gibt einen umfassenden Überblick über diese Erkrankung für erstbehandelnde tierärztliche Praxen.

Hypertrophe Kardiomyopathie (HCM) ist die häufigste Herzmuskelerkrankung bei Katzen, charakterisiert durch eine linksventrikuläre Hypertrophie und eine reduzierte diastolische Funktion.
Der Nachweis eines Herzgeräusches, einer Arrhythmie oder eines Galopprhythmus bei einer asymptomatischen Katze rechtfertigt immer eine weiterführende kardiologische Diagnostik.
Herzultraschall ist der Goldstandard der Diagnostik, wobei die Größe des linken Atriums ein wichtiger prognostischer Indikator ist.
HCM ist von einem variablen Fortschreiten gekennzeichnet und hat oft eine lange präklinische Phase: Das Staging liefert prognostische Informationen und hilft zu entscheiden, ob eine Behandlung oder eine Modifikation des Managements notwendig ist.
Bei der felinen hypertrophen Kardiomyopathie (HCM) handelt es sich um eine primäre Herzmuskelerkrankung, definiert durch eine linksventrikuläre konzentrische Hypertrophie, das heißt, eine Verdickung der Wände des linken Ventrikels 1. Es handelt sich um eine diastolische Dysfunktion (eingeschränkte Relaxation), normalerweise bei erhaltener systolischer Funktion (Kontraktilität). Die reduzierte Compliance des Myokards beeinträchtigt die Fähigkeit des Herzes, sich während der Diastole zu entspannen und zu füllen, wodurch der diastolische Druck steigt mit der Folge einer progredienten linksatrialen Dilatation 2. HCM ist eine Ausschlussdiagnose, das heißt, andere mögliche kardiale oder systemische Erkrankungen, die eine HCM verursachen oder zu einem HCM-Phänotyp beitragen können, müssen differenzialdiagnostisch ausgeschlossen werden, wie zum Beispiel eine systemische Hypertonie, eine Hyperthyreose, eine Akromegalie und eine Aortenstenose. Das Fortschreiten der Erkrankung ist hochvariabler Natur, und oft durchlaufen betroffene Patienten eine längere Zeit andauernde asymptomatische präklinische Phase, die in vielen Fällen unentdeckt bleibt. Betroffene Katzen können im Anschluss an diese präklinische Phase klinische Symptome einer kongestiven Herzinsuffizienz (CHF), einer arteriellen Thrombembolie (TE) oder Arrhythmien entwickeln 2,3.
Die HCM ist die häufigste Herzmuskelerkrankung bei Katzen und betrifft Schätzungen zufolge zwischen 14,5 und 34 % der „gesunden“ Katzenpopulation 1,4. Die meisten Fälle treten bei Kurzhaar- und Langhaarhauskatzen auf 4, Rassen mit einer besonderen Prädisposition für HCM sind jedoch Perserkatzen, British Shorthair, Maine Coon, Ragdoll, Sphynx, Himalayakatzen und Bengalkatzen. Katzen können grundsätzlich in jedem Alter betroffen sein, insbesondere aber reinrassige Katzen werden zum Teil jedoch bereits in jungem Alter mit einer hochgradigen Erkrankung vorgestellt 4. Die HCM ist überrepräsentiert bei männlichen Katzen, die für 75 % aller Fälle stehen, während ein geschlechtsassoziiertes erbliches Muster bislang nicht identifiziert werden konnte.
Catheryn Partington
Eine familiäre HCM bei den Rassen Maine Coon, Ragdoll und Sphynx 5,6,7 ist eine Folge von Mutationen in Sakromerproteinen. Bei allen anderen betroffenen Katzen ist die Ursache nach wie vor aber nicht bekannt, obgleich wahrscheinlich auch bei anderen reinrassigen Katzen eine Erblichkeit vorliegt. Das Sakromer ist die kleinste kontraktile Einheit der Herzmuskelzellen. Mutationen der Sarkomerproteine führen zu Veränderungen der Struktur und der Funktion der Sarkomere, die letztlich eine Einschränkung der Leistungsfähigkeit der Herzmuskelzellen zur Folge haben. Der exakte Prozess, über den eine Dysregulation der Sarkomere zu einem HCM-Phänotyp führt ist sehr komplex und wird bis heute noch nicht vollumfänglich verstanden. Veränderungen der Calciumsensitivität und der mechanischen Funktion sowie Zellstress kulminieren in einer Myozytenhypertrophie, einer Kollagensynthese und einer Myozytenunordnung – den histopathologischen Kennzeichen der felinen HCM 4,8.
Zwei unterschiedliche Mutationen des Myosinbindungsproteins in den Sarkomeren wurden bei den Rassen Maine Coon bzw. Ragdoll nachgewiesen (A31P bzw. R820W) 5,6. Individuen, die für diese Mutation heterozygot sind, haben oft eine subklinische Erkrankung mit Veränderungen ausschließlich auf zellulärer Ebene und nicht auf makroskopischer Ebene, während homozygote Katzen in der Regel hochgradiger betroffen sind. Vermutet wird ein Vererbungsmodus mit inkompletter Dominanz. Die Tatsache, dass auch Maine Coon Katzen ohne diese Mutation einen HCM-Phänotyp entwickeln können, spiegelt wahrscheinlich die multifaktorielle Ätiologie dieser Erkrankung wider. Jüngst wurde eine Mutation des ALMS1*-Gens als kausaler Faktor für HCM bei Sphynx-Katzen gefunden 7.
* ALMS1 = Alström-Syndrom 1
Wie oben erläutert manifestiert sich die HCM bei der Katze als linksventrikuläre Hypertrophie und diastolische Dysfunktion, wobei pathologische Veränderungen die Fähigkeit des Ventrikels verändern, sich während der Diastole zu entspannen und zu füllen. Zudem schränkt die progrediente Hypertrophie der Wand die Blutversorgung der Herzmuskelzellen ein. Wenn Herzmuskelzellen absterben, werden sie durch fibrotisches Gewebe ersetzt, wodurch sich die myokardiale Compliance weiter verschlechtert (vermehrte Steifheit des Myokards). In der Folge steigt der diastolische Druck im linken Ventrikel bei jedem gegebenen Blutvolumen, was wiederum zu einer Steigerung des Drucks im linken Atrium führt, das sich infolgedessen vergrößert. Ein erhöhter Druck im linken Atrium wird retrograd in die Lungenvenen übertragen, und wenn der Lungenvenendruck einen Wert von 25 mmHg übersteigt, bildet sich schließlich ein Lungenödem, das charakteristische Merkmal einer linksseitigen kongestiven Herzinsuffizienz 4. Bei der Katze münden die für die Drainage der Lungenpleura zuständigen Venen in die Pulmonalvenen, so dass sich bei linksseitiger kongestiver Herzinsuffizienz ein Pleuraerguss entwickeln kann (im Unterschied zum Hund, wo Pleuraergüsse immer die Folge einer rechtsseitigen kongestiven Herzinsuffizienz sind, und niemals einer linksseitigen) 4.
Eine progrediente Vergrößerung des linken Atriums ist einer der Faktoren, der Katzen mit HCM für die Entwicklung einer Thrombembolie prädisponiert, eine Erkrankung, deren weitere Besprechung jedoch außerhalb des Rahmens dieses Artikels liegt. Die ausgeprägte Hypertrophie, die reduzierte Sauerstoffversorgung der Herzmuskelzellen und die Ersatzfibrose im Myokard wirken dann gewissermaßen als Substrate für die Entwicklung von Arrhythmien.
Die Hypertrophie des linken Ventrikels bei Katzen mit HCM kann sowohl das interventrikuläre Septum als auch die freie Wand einbeziehen oder aber asymmetrische Veränderungen hervorrufen, die nur eine fokale Region betreffen – im typischen Fall die Basis des interventrikulären Septums. Die Hypertrophie kann aber auch den rechten Ventrikel betreffen, und das Muster und die Verteilung der Veränderungen können von Individuum zu Individuum in ganz erheblichem Maße variieren (Abbildung 1 und 2) 4. Veränderungen können auch am Mitralklappenapparat auftreten, wie zum Beispiel eine Verlängerung des anterioren Mitralklappensegels und eine Hypertrophie der Papillarmuskeln. Eine systolische Vorwärtsbewegung (SAM = systolic anterior movement) der Mitralklappe ist ein häufiges Merkmal der HCM bei Katzen und kann eine signifikante Obstruktion des linksventrikulären Ausflusstraktes (LVOTO) hervorrufen 9,10.


Abbildung 1. Bei einer felinen hypertrophen Kardiomyopathie kann das Muster der Hypertrophie des linken Ventrikels von Katze zu Katze erheblich variieren. Diese makroskopischen Befunde zeigen eine diffuse linksventrikuläre Hypertrophie.
Abkürzungen: LVFW: freie Wand des linken Ventrikels; IVS: interventrikuläres Septum; RV: rechter Ventrikel
Courtesy of Emanuele Ricci, University of Liverpool, UK.

Abbildung 2a. Die echokardiographischen Befunde der HCM zeigen eine große Variabilität. Ein rechter parasternaler Fünfkammerblick in der Längsachse zeigt eine fokale hypertrophe Region am basalen Septum (*).
Credit: Catheryn Partington – Joanna Dukes-McEwan

Abbildung 2b. Die echokardiographischen Befunde der HCM zeigen eine große Variabilität. Ein rechter parasternaler Kurzachsenblick auf der Ebene der Papillarmuskeln zeigt eine linksventrikuläre Hypertrophie und eine Papillarmuskelhypertrophie.
Credit: Catheryn Partington – Joanna Dukes-McEwan

Abbildung 2c. Die echokardiographischen Befunde der HCM zeigen eine große Variabilität. Ein rechter parasternaler Vierkammerblick in der Längsachse zeigt eine symmetrische Hypertrophie des interventrikulären Septums und der freien Wand des linken Ventrikels.
Credit: Catheryn Partington – Joanna Dukes-McEwan
Abkürzungen: LA: linkes Atrium; LV: linker Ventrikel; Pm: Papillarmuskel
Eine Untergruppe von Katzen mit HCM kann eine signifikante LVOTO aufweisen (Abbildung 3). In diesen Fällen wird die Erkrankung klassischerweise als hypertrophe obstruktive Kardiomyopathie (HOCM) bezeichnet. In der Humanmedizin ist man von diesem Begriff aufgrund des möglichen intermittierenden Auftretens der Veränderung inzwischen jedoch wieder abgekommen, und da dies auch bei Katzen zutrifft, dürfte der Begriff HOCM auch bei dieser Spezies veraltet sein 3,9,11. Eine LVOTO kann die Folge einer systolischen Vorwärtsbewegung der Mitralklappe, einer fokalen Hypertrophie des basalen Septums oder – seltener – einer Obstruktion im mittleren Bereich der Kammer („mid-cavity obstruction“) aufgrund einer Papillarmuskelhypertrophie sein 4,9,12. Aufgrund von Turbulenzen des Blutflusses verursacht die LVOTO ein Herzgeräusch. Bei systolischer Vorwärtsbewegung der Mitralklappe ist die Obstruktion im typischen Fall dynamischer Natur und verstärkt sich bei erhöhter kardialer Kontraktilität, zum Beispiel während einer körperlichen oder emotionalen Stressbelastung. In vielen Fällen liegt hier der Grund für das unregelmäßige Auftreten und die variable Intensität von Herzgeräuschen bei Katzen mit HCM.
Eine systolische Vorwärtsbewegung der Mitralklappe entsteht, wenn das septale (anteriore) Segel (oft verlängert) in Richtung des Ausflusstraktes gezogen wird. Es handelt sich um die Folge einer Hypertrophie und Verlagerung des Papillarmuskels, der dadurch schlaffe Chordae tendinae aufweist 10. Mit der Verengung des Ausflusstraktes infolge dieser abnormen Bewegung des Segels (oder infolge einer Hypertrophie des basalen Septums) steigt die Geschwindigkeit des Blutflusses, und der Druck nimmt zu, was wiederum dazu führt, dass die Spitze des Segels noch weiter in den Ausflusstrakt hineingezogen wird, wodurch sich die Obstruktion weiter verstärkt (Venturi-Effekt) 4,9. Man geht davon aus, dass die systolische Vorwärtsbewegung der Mitralklappe letztlich den Sauerstoffbedarf des Myokards steigert und die koronare Durchblutung mindert, wodurch wiederum das Risiko einer myokardialen Ischämie zunimmt. Wahrscheinlich besteht hier ein Zusammenhang mit einer progredienten Hypertrophie und einer mikrovaskulären Dysfunktion. Vermutlich zeigen einige Katzen mit hochgradiger LVOTO Symptome einer verminderten Leistungskapazität und Angina-artige Schmerzen, wie dies auch bei Menschen beschrieben wird.

Abbildung 3a. Herzgeräusche bei Katzen mit HCM sind oft die Folge einer Obstruktion des linksventrikulären Ausflusstraktes (LVOTO). Ein rechter parasternaler Fünfkammerblick im Farbdoppler zeigt einen turbulenten Blutfluss vom linksventrikulären Ausflusstrakt (offener Pfeil), verursacht durch die systolische Vorwärtsbewegung der Mitralklappe und einen kleinen exzentrischen Jet einer Mitralregurgitation (kleiner Pfeil).
Credit: Catheryn Partington – Joanna Dukes-McEwan

Abbildung 3b. Herzgeräusche bei Katzen mit HCM sind oft die Folge einer Obstruktion des linksventrikulären Ausflusstraktes (LVOTO). Ein rechter parasternaler Fünfkammerblick in der Längsachse zeigt eine fokale Hypertrophie im basalen Septum (*) als eine Ursache von LVOTO.
Credit: Catheryn Partington – Joanna Dukes-McEwan

Abbildung 3c. Herzgeräusche bei Katzen mit HCM sind oft die Folge einer Obstruktion des linksventrikulären Ausflusstraktes (LVOTO). Dieser Spektral-Doppler-Befund des LVOT zeigt erhöhte Geschwindigkeiten (*) und eine biphasische Beschleunigung (klassische „Scimitar“-Form), auf eine LVOTO hinweisend.
Courtesy of J. Novo Matos, University of Cambridge, UK.
Abkürzungen: Ao: Aorta; LA: linkes Atrium; LV: linker Ventrikel
Die transiente mykokardiale Verdickung (Transient Myocardial Thickening = TMT) ist eine wichtige Differenzialdiagnose für einen HCM-Phänotyp. Diese Erkrankung kommt nur selten vor und wird bislang nur wenig verstanden. Sie ist gekennzeichnet durch Dickenzunahmen der Wand des linken Ventrikels und eine linksventrikuläre Dilatation, die insgesamt aber weniger deutlich ausgeprägt sind als bei der primären HCM. Über einen Zeitraum von einigen Monaten kommt es zu einer vollständigen Resolution der klinischen Symptome und der echokardiographischen Veränderungen. In der Regel geht eine transiente myokardiale Verdickung also mit einer hervorragenden Prognose einher. Katzen mit sekundärer kongestiver Herzinsuffizienz infolge einer transienten myokardialen Verdickung sind tendenziell jünger als ihre Artgenossen mit primärer HCM, und in vielen Fällen wird ein vorangegangenes Ereignis beschrieben (z. B. eine Allgemeinanästhesie). Postuliert wird, dass die vermehrte Wanddicke bei den betroffenen Katzen die Folge eines Myokardödems sein könnte, und man erkennt hier Ähnlichkeiten mit der akuten Myokarditis und der stressinduzierten Kardiomyopathie bei Menschen 13.
Die aktuellen ACVIM-Leitlinien zur Diagnose und Behandlung der HCM 14 beinhalten ein Staging-System, das der Klassifikation der myxomatösen Mitralklappenerkrankung beim Hund ähnelt (Box 1). Dieses System unterstützt die Beantwortung der Frage, ob im Einzelfall eine Behandlung angezeigt ist und gibt Besitzern gewisse Hinweise darauf, was sie zu erwarten haben, da das Fortschreiten der HCM und somit die Prognose letztlich hochgradig variabel sind. Bei einigen Katzen ist die Erkrankung progredient und führt zu kongestiver Herzinsuffizienz, Thrombembolie und kardialem Tod, während andere betroffene Katzen präklinisch bleiben und eventuell an nicht-kardialen Ursachen sterben 14,15. Der Grund für diese Heterogenität der Schweregrade und klinischen Verläufe ist nach wie vor unklar, und es bleibt schwierig, vorherzusagen, welche Katzen ihrer Erkrankung letztlich erliegen werden und welche nicht. In mehreren retrospektiven Studien konnten jedoch einige prognostische Faktoren identifiziert werden. So haben Katzen, bei denen die Diagnose bereits in einem früheren Alter gestellt wird, tendenziell längere Überlebenszeiten 2. Und Katzen, die eine sekundäre kongestive Herzinsuffizienz aufgrund von Faktoren wie Stress oder intravenöser Flüssigkeitstherapie entwickeln und damit in das Stadium C übergehen, haben gewöhnlich längere Überlebenszeiten als andere Katzen mit HCM im Stadium C. Dagegen gehen klinische Befunde wie ein Galopprhythmus, Arrhythmien, eine hochgradige Dilatation des linken Atriums, eine reduzierte systolische Funktion des linken Atriums, Spontankontrast, eine hochgradige Wandhypertrophie (> 9 mm), eine systolische Dysfunktion des linken Ventrikels und fokale Wandverdickungen mit einem erhöhten Risiko für die Entwicklung einer kongestiven Herzinsuffizienz und/oder einer Thrombembolie einher 2,15.
Box 1. ACVIM-Staging der felinen HCM.
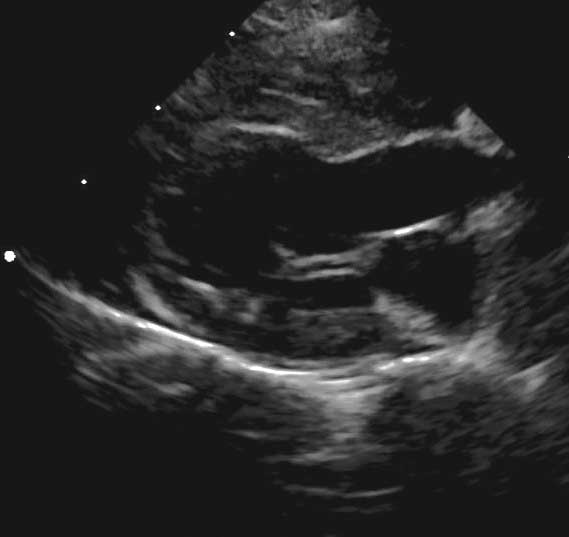 |
Stadium A |
Stadium A: Katzen mit Prädisposition, aber ohne aktuell vorhandene Symptome einer HCM; z. B. eine Maine Coon mit der A31P-Genmutation, oder eine Katze, bei deren engen Verwandten eine HCM diagnostiziert wurde. Im Herzultraschall erscheint das Herz strukturell physiologisch. |
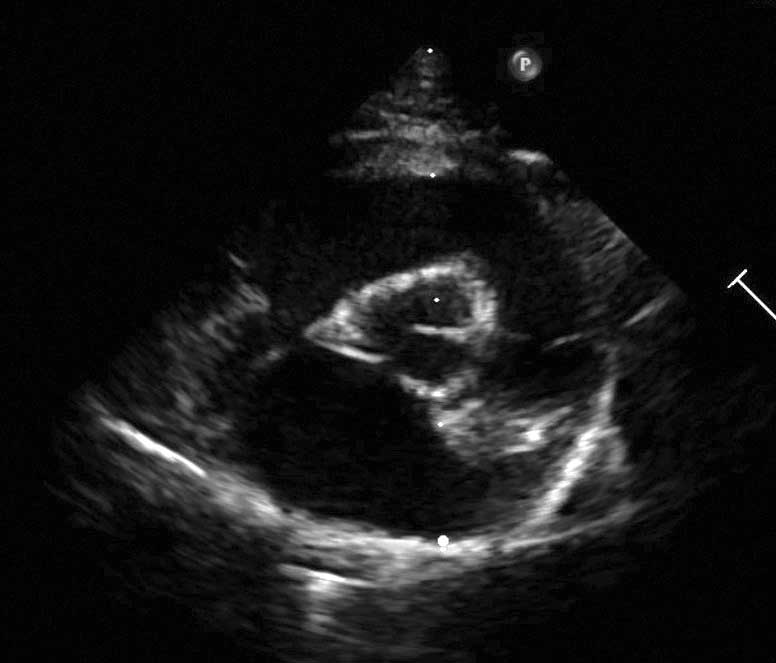 |
Stadium B1 |
Stadium B: Katzen mit präklinischer HCM (d. h., keine klinischen Symptome, aber echokardiographische Hinweise auf HCM). Dieses Stadium wird weiter unterteilt auf der Basis des Grades der Erkrankung und des Risikos für die Entwicklung von kongestiver Herzinsuffizienz (CHF) und Thrombembolie (TE).
|
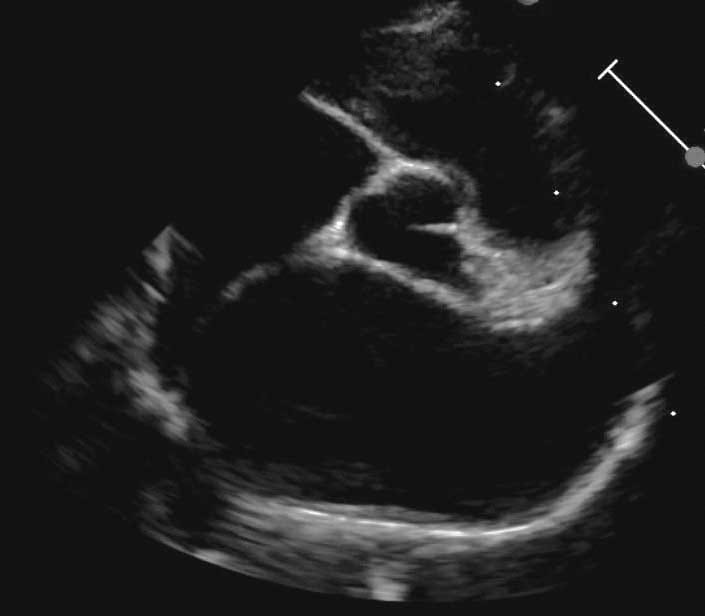 |
Stadium B2 | |
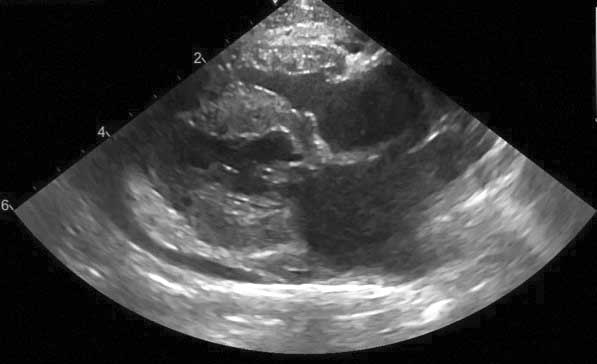 |
Stadium C | Stadium C: Katzen mit klinischen Symptomen einer HCM und CHF oder TE. |
 |
Stadium D |
Stadium D: HCM-Katzen mit therapieresistenter CHF.
|
Credit: Catheryn Partington
Aufgrund der reduzierten diastolischen Funktion und des dadurch bedingten Druckanstieges für jedes gegebene Blutvolumen im linken Ventrikel sind Katzen mit HCM insgesamt empfindlicher für Anstiege des zirkulierenden Volumens (d. h., erhöhte Vorlast). Bestimmte Behandlungen, wie zum Beispiel die längere Gabe von Kortikosteroiden und eine intravenöse Flüssigkeitstherapie können bei einer Katze mit fortgeschrittener HCM deshalb eine Entwicklung in Richtung einer linksseitigen kongestiven Herzinsuffizienz forcieren. Dies unterstreicht, wie wichtig es ist, Katzen mit präklinischer Erkrankung zu identifizieren, um solche Behandlungen entsprechend modifizieren und eng überwachen zu können (z. B. Senkung der Infusionsrate, engere Überwachung der Atemfrequenz und bildgebende Verlaufsuntersuchung zur Beurteilung der Größe des linken Atriums), mit dem Ziel, das Risiko einer Dekompensation zu verringern. Da Katzen mit fortgeschrittener HCM darüber hinaus ein erhöhtes Thrombembolie-Risiko aufweisen, ermöglicht das rechtzeitige Erkennen solcher Patienten die frühzeitige Einleitung einer präventiven gerinnungshemmenden Therapie.
Die Identifizierung von Katzen mit HCM bereits im Stadium B kann das Erkennen von subtilen klinischen Symptomen eines frühen Fortschreitens in Richtung Stadium C erleichtern, da Besitzer in diesen Fällen besser geschult werden können und aufmerksamer auf etwaige Symptome einer kongestiven Herzinsuffizienz achten. Dies wiederum ermöglicht die frühzeitige Einleitung einer Therapie, noch bevor der Patient ein signifikantes Lungenödem und eine hochgradige Einschränkung der Atmung entwickelt.
Die große Herausforderung bei der HCM liegt in der unterschiedlichen Länge der präklinischen Phase und dem häufigen Fehlen jeglicher klinischer Symptome bei der klinischen Untersuchung. Veränderungen bei der klinischen Untersuchung, die den Verdacht auf eine HCM im Stadium B aufkommen lassen sollten, sind Herzgeräusche (Box 2), ein Galopprhythmus (Box 3) oder eine Arrhythmie 4. Während aber viele Katzen mit HCM tatsächlich ein Herzgeräusch aufweisen, wird bei bis zu 31-62 % dieser Patienten kein Herzgeräusch festgestellt, und 25-33% der Katzen mit linksseitigen, parasternalen systolischen Geräuschen (im typischen Fall ein weiches Geräusch geringen Grades) zeigen keine echokardiographischen Hinweise auf eine Kardiomyopathie 1,4. Herzgeräusche höherer Intensität (> Grad 3/6) stehen mit höherer Wahrscheinlichkeit im Zusammenhang mit einer signifikanteren Herzerkrankung 4, grundsätzlich rechtfertigt aber jedes Herzgeräusch bei einer Katze eine weiterführende kardiologische Diagnostik.
Box 2. Ursachen von Herzgeräuschen bei Katzen mit präklinischer HCM.
|
Herzgeräusche entstehen, wenn der Blutfluss Turbulenzen aufweist. Mögliche Ursachen von Turbulenzen sind eine hohe Geschwindigkeit des Blutflusses, ein großer Gefäßdurchmesser, eine hohe Flüssigkeitsdichte oder eine niedrige Viskosität. Bei HCM sind Herzgeräusche meist das Ergebnis einer Obstruktion des linksventrikulären Ausflusstraktes (LVOTO) aufgrund einer systolischen Vorwärtsbewegung der Mitralklappe und/oder einer fokalen Hypertrophie des basalen Septums.
|
Box 3. Was ist ein Galopprhythmus?
|
Bei den meisten gesunden Katzen und Hunden sind bei der Auskultation nur der erste Herzton (S1) und der zweite Herzton (S2) zu hören. Bei einem Galopprhythmus gibt es einen hörbaren dritten Herzton, so dass eine dreifache Kadenz entsteht, die dem Hufschlag eines galoppierenden Pferdes ähnelt.
Die Ursache ist entweder ein hörbarer dritter Herzton (S3) oder ein vierter Herzton (S4), wobei eine auskultatorische Unterscheidung zwischen diesen beiden oft schwierig ist. S3 ist das Ergebnis einer schnellen ventrikulären Füllung in der frühen Diastole, während S4 die Folge einer aktiven ventrikulären Füllung über eine atriale Kontraktion in der späten Diastole ist.
Der auskultatorische Befund eines Galopprhythmus weist im Allgemeinen auf eine diastolische Dysfunktion hin, und 2,6-19 % der Katzen mit subklinischer HCM weisen einen Galopprhythmus auf 19. Galopprhythmen werden bei gesunden Katzen nur selten festgestellt, ein entsprechender Nachweis sollte also immer weiterführende kardiologische Untersuchungen nach sich ziehen.
|
Credit: Catheryn Partington – Joanna Dukes McEwan
Herzultraschall ist der Goldstandard der Diagnose einer HCM 14, und wenn sonographisch eine Hypertrophie festgestellt wird, sollten stets mögliche Ursachen einer sekundären Hypertrophie abgeklärt werden (siehe Teil 2). Eine Indikation für eine Herzultraschalluntersuchung besteht grundsätzlich bei jeder Katze mit klinischen Symptomen, die auf eine Kardiomyopathie zurückzuführen sein könnten (Synkope, Leistungsintoleranz, Unverträglichkeit einer intravenösen Flüssigkeitstherapie), bei Katzen mit familiärer Vorgeschichte einer HCM (oder plötzliche Todesfälle), bei reinrassigen Katzen, die für die Zucht vorgesehen sind, und schließlich bei Katzen, deren klinische Untersuchung Befunde liefert, die den Verdacht einer Kardiomyopathie aufkommen lassen (Galopprhythmus, Arrhythmien, Herzgeräusche, Tachypnoe, Dyspnoe, reduzierte Lungentöne). Das Consensus Statement des ACVIM empfiehlt zudem generell eine echokardiographische Beurteilung bei Katzen über neun Jahren, wenn diese Interventionen unterzogen werden, die die Entwicklung einer kongestiven Herzinsuffizienz fördern können (z. B. Allgemeinanästhesie, intravenöse Flüssigkeitstherapie und längere Kortikosteroidbehandlung) 14.
Bei der Echokardiographie asymptomatischer Katzen werden vier Hauptkriterien beurteilt: die Wanddicke des linken Ventrikels, die Größe des linken Atriums, das Vorhandensein von LVOTO und die diastolische Funktion. Bei Patienten mit mittel- bis hochgradiger Erkrankung können die ersten beiden Aspekte auch von Allgemeinpraktikern mit Basiswissen in der Echokardiographie relativ leicht beurteilt werden.
1. Wanddicke des linken Ventrikels
Beurteilt werden sowohl das interventrikuläre Septum als auch die freie Wand des linken Ventrikels. Gemessen wird mit der zweidimensionalen Echokardiographie in der rechten parasternalen Schnittebene in der Enddiastole (im Bild vor dem Verschließen der Mitralklappensegel) (Abbildung 4a). Da die Hypertrophie fokal begrenzt sein kann, sollten Messungen über mindestens drei Herzzyklen erfolgen und im Idealfall an verschiedenen Stellen. Sorgfältig sollte darauf geachtet werden, dass nicht Papillarmuskeln oder Bereiche mit ausgeprägter endokardialer Verdickung in die Messungen der Wanddicke einbezogen werden. Eine enddiastolische linksventrikuläre Wanddicke von weniger als 5 mm gilt als physiologisch, während Messwerte von ≥ 6 mm einer Hypertrophie entsprechen 14. Werte von 5-6 mm gelten als Grauzone und sollten stets unter Berücksichtigung der Körpergröße der Katze, der Rasse und anderer echokardiographischer Variablen interpretiert werden 16.

Abbildung 4a. Echokardiographische Beurteilung der hypertrophen Kardiomyopathie (HCM). Rechter parasternaler Fünfkammerblick in der Längsachse. Die Dicke der freien Wand des linken Ventrikels und des interventrikulären Septums sollten in zweidimensionalen Bildern in der Diastole gemessen werden; Werte ≥ 6 mm entsprechen einer Hypertrophie.
Credit: Catheryn Partington – Joanna Dukes-McEwan
2. Größe des linken Atriums
Die Größe des linken Atriums ist ein Risikofaktor für kongestive Herzinsuffizienz, Thrombembolie und kardialen Tod und kann sowohl in der rechten parasternalen Längsachse als auch in der rechten parasternalen Kurzachse beurteilt werden. In den Kurzachsenebenen auf Höhe der Herzbasis erfolgen die Messungen in der frühen Diastole (im Bild nach Verschluss der Aortenklappensegel), wobei der Durchmesser des Atriums mit der Aorta in Beziehung gesetzt wird (LA/Ao; Abbildung 4b). Die Messung der Aorta erfolgt vom Mittelpunkt der konvexen Kurvatur der Wand des rechten Aortensinus bis zu dem Punkt, an dem die Aortenwand, die nichtkoronaren und die linkskoronaren Aortensegel zusammenlaufen. Das linke Atrium wird von diesem letztgenannten Punkt bis zur freien Vorhofwand gemessen, wobei ein Eindringen in die Lungenvenen zu vermeiden ist 17.

Abbildung 4b. Echokardiographische Beurteilung der hypertrophen Kardiomyopathie (HCM). Rechter parasternaler Kurzachsenblick auf der Ebene der Herzbasis. Die Größe des linken Atriums wird ins Verhältnis zur Aortenwurzel gesetzt (LA/Ao), gemessen in der frühen Diastole; Werte > 1,6 entsprechen einer Dilatation des linken Atriums.
Credit: Catheryn Partington – Joanna Dukes-McEwan
Im Vierkammerblick in der rechten parasternalen Längsachse sollte das linke Atrium optimiert und der linksatriale Durchmesser (LAD) in der Endsystole gemessen werden (im Bild vor der Öffnung der Mitralklappensegel), indem man parallel zum Mitralring eine Linie zieht vom interatrialen Septum zur freien Vorhofwand (Abbildung 4c) 18. Ein LA/Ao-Quotient > 1,6 und ein LAD > 16,0 mm sprechen für eine Vergrößerung des linken Atriums, und ein LA/Ao-Quotient > 1,8-2,0 und ein LAD > 18-19 mm weisen auf eine mittel- bis hochgradige Vergrößerung des linken Atriums hin. Um die systolische Funktion zu beurteilen, kann auch die linksatriale fraktionelle Verkürzung evaluiert werden. Ebenfalls wichtige Faktoren für die Einschätzung des Risikos der Entstehung einer kongestiven Herzinsuffizienz und einer Thrombembolie sind eine subjektive Beurteilung der linksaurikulären Größe, das Vorhandensein eines Spontankontrasts oder eines Thrombus und die Beurteilung der linksaurikulären Strömungsgeschwindigkeiten.

Abbildung 4c. Echokardiographische Beurteilung der hypertrophen Kardiomyopathie (HCM). Rechter parasternaler Vierkammerblick in der Längsachse. Der Durchmesser des linken Atriums wird parallel zum Mitralring in der Endsystole gemessen; Werte > 16,0 mm sprechen für eine Dilatation des linken Atriums.
Credit: Catheryn Partington – Joanna Dukes-McEwan
Abkürzungen: Ao: Aorta; IVS: interventrikuläres Septum; LA: linkes Atrium; LV: linker Ventrikel; LVFW: freie Wand des linken Ventrikels; MV: Mitralklappe
3. Obstruktion des linksventrikulären Ausflusstraktes (LVOTO)
Das Vorhandensein einer LVOTO wird mit dem zweidimensionalen M-Mode Farb- und Spektraldoppler beurteilt (Abbildung 3c). Eine systolische Vorwärtsbewegung der Mitralklappe (SAM) kann sowohl mit der zweidimensionalen Sonographie als auch im M-Mode dargestellt werden. Der Farb-Doppler zeigt Turbulenzen im linksventrikulären Ausflusstrakt und möglicherweise eine Mitralregurgitation. Ein Spektral-Doppler zur Beurteilung der Strömungsgeschwindigkeiten im linksventrikulären Ausflusstrakt erfordert eine gute Ausrichtung zur Flussrichtung; bei dynamischer Obstruktion zeigt das Doppler-Profil oft eine biphasische Beschleunigung (eine klassische Scimitar-Form).
4. Diastolische Funktion
Die diastolische Funktion kann sowohl mit dem Spektral-Doppler als auch mit dem Gewebedoppler beurteilt werden, eine weitere Diskussion würde an dieser Stelle aber den Rahmen dieses Artikels sprengen. Katzen mit fortgeschrittener HCM können auch eine eingeschränkte systolische Funktion aufweisen.
Thoraxröntgen gilt als der Goldstandard der Diagnose eines Lungenödems, ist aber weniger hilfreich bei asymptomatischen Katzen 14. Zu erkennen sein kann eine hochgradige Kardiomegalie mit einem vorgewölbten linken Atrium. Insgesamt besitzen Röntgenaufnahmen aber eine geringere Sensitivität für den Nachweis eines gering- bis mittelgradigen Remodellings bei HCM-Patienten, die in vielen Fällen eine physiologische Herzsilhouette aufweisen können.
Biomarker werden an anderer Stelle im Detail diskutiert, kurz zusammengefasst kann aber festgestellt werden, dass sie als nützliche diagnostische Werkzeuge in Kombination mit anderen diagnostischen Maßnahmen eingesetzt werden können oder zur Überwachung des Fortschreitens der Erkrankung dienen. Als Screening-Tool sollten kardiale Biomarker aber nur mit Vorsicht eingesetzt werden. Bei asymptomatischen Katzen hat quantitatives NT-proBP (ein Marker für myokardialen Stress und myokardiale Dehnung) nur einen geringen Nutzen als Screening-Tool in der allgemeinen Population, da es zwar eine hohe Spezifität aufweist, die Sensitivität aber relativ niedrig ist, so dass ein hohes Risiko für falsch-negative Ergebnisse besteht. Besser geeignet ist dieser Test wahrscheinlich eher in speziell ausgewählten Fällen mit konkretem Verdacht auf eine Kardiomyopathie (d. h., wenn ein Herzgeräusch nachweisbar ist) 19, und zusammen mit der Echokardiographie für eine bessere Einschätzung des Schweregrades einer Kardiomyopathie. Bei symptomatischen Katzen hat der praxisinterne NT-proBP-Test einen größeren Nutzen zur Unterscheidung zwischen kardialen und extrakardialen Ursachen einer Dyspnoe 20.
Kardiales Troponin I (Tn I) – ein Marker für Herzmuskelzellschäden – ist in Kombination mit der Echokardiographie hilfreich, und hat Untersuchungen zufolge eine prognostische Bedeutung, wobei erhöhte Werte mit schlechteren Outcomes assoziiert sind 21. Zu hohen Troponin-I-Werten kann eine myokardiale Ischämie führen, die bei Katzen mit fortgeschrittener HCM beschrieben wird. Hochgradige Anstiege dieses Markers sind verdächtig für eine Myokarditis, die einen sekundären HCM-Phänotyp hervorruft und eine weitere diagnostische Abklärung rechtfertigt.
Bei Katzen mit systolischer Vorwärtsbewegung der Mitralklappen (SAM) sind die Konzentrationen von Biomarkern nachweislich höher als bei Katzen ohne SAM, und zwar selbst bei Katzen mit physiologischer oder zweifelhafter Größe des Atriums 22.
Genetische Tests sind für die Rassen Maine Coon, Ragdoll und Sphynx (Abbildung 5) verfügbar und werden insbesondere für sämtliche Zuchtkatzen dieser Rassen empfohlen, um die erbliche Prävalenz der HCM zu reduzieren. Von einer Zucht mit Individuen, die für diese Mutation homozygot sind, wird abgeraten, während heterozygote Individuen mit Tieren gepaart werden können, die für diese Mutation negativ sind 14. Züchter sollten sich aber darüber im Klaren sein, dass auch Katzen ohne Nachweis der bekannten genetischen Mutationen eine HCM entwickeln können.

Abbildung 5. Tierärzte in erstbehandelnden Praxen sollten bei ihren Patienten sehr aufmerksam auf Symptome einer HCM achten, und die Untersuchung einer Katze sollte immer eine sorgfältige Auskultation auf Herzgeräusche, Galopprhythmus und Arrhythmien beinhalten, da jeder einzelne dieser Befunde weiterführende diagnostische Maßnahmen rechtfertigt. Insbesondere gilt dies bei Katzenrassen mit bekannter Neigung zu Kardiomyopathien, und heute gibt es Tests zum Nachweis der genetischen Mutation, die bei Sphynx-Katzen für HCM verantwortlich sein kann.
Credit: Shutterstock
Das Staging von Katzen mit HCM kann die Standardisierung der Behandlung unterstützen. Keine Behandlung ist bei Katzen im Stadium A und im Stadium B1 (keine oder nur minimale linksatriale Dilatation) erforderlich, außer in Fällen mit hochgradiger LVOTO, in denen die Gabe von Beta-Blockern in Betracht gezogen werden kann (siehe unten). Aufgrund des Risikos für einen Thrombembolie ist bei Katzen mit Stadium B2 die Gabe von Clopidogrel als präventive Therapie angezeigt. Die Behandlung von Katzen mit HCM im Stadium C und im Stadium D wird im zweiten Teil diskutiert.
Wie bei der HCM des Menschen sind Insulin, Insulin-Like Growth Factor-1 und Entzündungen wahrscheinlich an der Pathophysiologie der felinen HCM beteiligt. Diätetische Modifikationen, die spezifisch auf diese Faktoren abzielen, könnten deshalb vorteilhafte Effekte haben. So zeigt zum Beispiel eine Studie, dass Katzen mit präklinischer HCM, die eine Nahrung mit reduziertem Stärkegehalt und einer Omega-3-Fettsäuresupplementierung erhielten, ein reduziertes Remodelling des linken Ventrikels aufwiesen. Sollten solche kardialen Diätnahrungen in der Zukunft kommerziell erhältlich sein, könnten sie als eine therapeutische Maßnahme bei Katzen mit HCM im Stadium B in Betracht gezogen werden 23.
Bei Menschen mit HCM und hochgradiger LVOTO werden häufig eine Leistungsintoleranz und Angina beschrieben, deren klinische Symptome sich nach einer Therapie mit Beta-Blockern verbessern. Bei Katzen mit Hinweisen auf LVOTO bleibt die Anwendung von Beta-Blockern dagegen umstritten, und die Autorinnen empfehlen, entsprechende Fälle für diese Entscheidung an einen Kardiologen zu überweisen. Theoretisch erscheinen Beta-Blocker in hochgradigen LVOTO-Fällen vorteilhaft, da die negativen inotropen und chronotropen Effekte dieser Wirkstoffe den Grad der Obstruktion lindern können und gleichzeitig die Sauerstoffversorgung des Myokards verbessern, wodurch letztlich das Risiko für die Entwicklung von Arrhythmien und einer Ischämie sinkt. Entsprechende Vorteile für das Langzeitüberleben oder die Lebensqualität bei Katzen konnten bislang aber nicht festgestellt werden 24,25. Darüber hinaus sind Beta-Blocker in Fällen einer kongestiven Herzinsuffizienz kontraindiziert und wären bei Katzen, die sich einer Dekompensation nähern, wahrscheinlich schädlich.
Joanna Dukes-McEwan
In Anbetracht der hohen Prävalenz der HCM bei Katzen und der Tendenz zu einer länger anhaltenden präklinischen Phase sowie der Gefahr einer Entwicklung hochgradiger klinischer Symptome, sollten Allgemeinpraktiker bei ihren felinen Patienten stets sehr aufmerksam auf mögliche Symptome einer Erkrankung im Stadium B achten. Jede klinische Untersuchung bei einer Katze sollte deshalb eine sorgfältige Auskultation auf Herzgeräusche, Galopprhythmus und Arrhythmien beinhalten, da jeder einzelne dieser Befunde weiterführende Untersuchungen rechtfertigt. Die Identifizierung von Katzen mit HCM im Stadium B ermöglicht die Einleitung einer präventiven Therapie, wo dies praktikabel ist, bietet aber auch die Gelegenheit für ein gezieltes Risikomanagement im Vorfeld von Interventionen oder Behandlungen, die eine Dekompensation fördern könnten. Auch eine verbesserte Schulung und eine vermehrte Aufmerksamkeit der Besitzer können die Diagnose einer kongestiven Herzinsuffizienz noch vor der Entwicklung einer hochgradigen Einschränkung der Atmung erleichtern.
Payne JR, Brodbelt DC, Luis Fuentes V. Cardiomyopathy prevalence in 780 apparently healthy cats in rehoming centres (the CatScan study). J. Vet. Cardiol. 2015;17 Suppl 1:S244-S257.
Fox PR, Keene BW, Lamb K, et al. International collaborative study to assess cardiovascular risk and evaluate long-term health in cats with preclinical hypertrophic cardiomyopathy and apparently healthy cats: the REVEAL study. J. Vet. Intern. Med. 2018;32:930-943.
Kittleson MD, Cote E. The feline cardiomyopathies: 2. Hypertrophic Cardiomyopathy. J. Feline Med. Surg. 2021;23:1028-1051.
Cote E, MacDonald KA, Meurs KM, et al. Hypertrophic Cardiomyopathy. In: Feline Cardiology. 1st ed. John Wiley & Sons, Inc. 2011 Chapter 11;101-175.
Meurs KM, Sanchez X, David RM, et al. A cardiac myosin binding protein C mutation in the Maine Coon cat with familial hypertrophic cardiomyopathy. Hum. Mol. Genet. 2005;14:3587-3593.
Meurs KM, Norgard MM, Ederer MM, et al. A substitution mutation in the myosin binding protein C gene in Ragdoll hypertrophic cardiomyopathy. Genomics 2007;90:261-264.
Meurs KM, Williams BG, de Prospero D, et al. A deleterious mutation in the ALMS1 gene in a naturally occurring model of hypertrophic cardiomyopathy in the Sphynx cat. Orphanet J. Rare Dis. 2021;16:108.
Kittleson MD, Meurs KM, Harris SP. The genetic basis of hypertrophic cardiomyopathy in cats and humans. J. Vet. Cardiol. 2015;17 Suppl 1:S53-S73.
Schober K, Todd A. Echocardiographic assessment of left ventricular geometry and the mitral valve apparatus in cats with hypertrophic cardiomyopathy. J. Vet. Cardiol. 2010;12:1e16.
Seo J, Novo Matos J, Payne JR, et al. Anterior mitral valve leaflet length in cats with hypertrophic cardiomyopathy. J. Vet. Cardiol. 2021;37:62-70.
Maron BJ, Maron MS. A discussion of contemporary nomenclature, diagnosis, imaging, and management of patients with hypertrophic cardiomyopathy. Am. J. Cardiol. 2016;118:1897-1907.
MacLea HB, Boon JA, Bright JM. Doppler echocardiographic evaluation of mid ventricular obstruction in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2013;27:1416-1420.
Novo Matos J, Pereira N, Glaus T, et al. Transient myocardial thickening in cats associated with heart failure. J. Vet. Intern. Med. 2018;32(1):48-56.
Luis Fuentes V, Abbott J, Chetboul V, et al. ACVIM consensus statement guidelines for the classification, diagnosis, and management of cardiomyopathies in cats. J. Vet. Intern. Med. 2020;34:1062-1077.
Payne JR, Borgeat K, Connolly DJ, et al. Prognostic indicators in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2013;27:1427-1436.
Haggstrom J, Andersson AO, Falk T, et al. Effect of body weight on echocardiographic measurements in 19,866 pure-bred cats with or without heart disease. J. Vet. Intern. Med. 2016;30:1601-1611.
Hansson K, Haggstrom J, Kvart C, et al. Left atrial to aortic root indices using two-dimensional and M-mode echocardiography in Cavalier King Charles Spaniels with and without left atrial enlargement. Vet. Radiol. Ultrasound 2002;43(6):569-575.
Linney CJ, Dukes-McEwan J, Stephenson HM, et al. Left atrial size, atrial function and left ventricular diastolic function in cats with hypertrophic cardiomyopathy. J. Small. Anim. Pract. 2014;55(4):198-206.
Fox PR, Rush JE, Reynolds CA, et al. Multicenter evaluation of plasma N-terminal probrain natriuretic peptide (NT-pro BNP) as a biochemical screening test for asymptomatic (occult) cardiomyopathy in cats. J. Vet. Intern. Med. 2011;25:1010-1016.
Ward JL, Lisciandro GR, Ware WA, et al. Evaluation of point-of-care thoracic ultrasound and NT-proBNP for the diagnosis of congestive heart failure in cats with respiratory distress. J. Vet. Intern. Med. 2018;32:1530-1540.
Borgeat K, Sherwood K, Payne J, et al. Plasma cardiac troponin I concentration and cardiac death in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2014;28:1731-1737.
Seo J, Payne JR, Novo Matos J, et al. Biomarker changes with systolic anterior motion of the mitral valve in cats with hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2020;34(5):1718-1727.
van Hoek I, Hodgkiss-Geere H, Bode EF, et al. Association of diet with left ventricular wall thickness, troponin I and IGF-1 in cats with subclinical hypertrophic cardiomyopathy. J. Vet. Intern. Med. 2020;34(6):2197-2210.
Schober KE, Zientek J, Li X, et al. Effect of treatment with atenolol on 5-year survival in cats with preclinical (asymptomatic) hypertrophic cardiomyopathy. J. Vet. Cardiol. 2013;15:93-104.
Coleman AE, DeFrancesco TC, Griffiths EH, et al. Atenolol in cats with subclinical hypertrophic cardiomyopathy: a double-blind, placebo-controlled, randomized clinical trial of effect on quality of life, activity, and cardiac biomarkers. J. Vet. Cardiol. 2020;30:77-91.
Catheryn Partington
Dr. Partington schloss ihr Tiermedizinstudium 2014 an der University of Liverpool ab und erhielt zudem einen Master in Veterinary Science, bevor sie an die University of Liverpool zurückkehrte für ein rotierendes Internship und eine Residency im Bereich Kardiologie, die sie im Jahr 2021 abschloss Mehr lesen
Joanna Dukes-McEwan
Professor Dukes-McEwan schloss ihr Tiermedizinstudium 1986 an der University of Glasgow ab und absolvierte dort anschließend ein Internship und eine Residency Mehr lesen
Lungenwürmer und Herzwürmer sind eine unterschätzte, aber potenziell ernste Bedrohung für viele Katzen, wie uns dieser Artikel erläutert.
Eine Zwerchfellhernie ist eine häufige Folge traumatischer Verletzungen bei Katzen und kann tödlich enden, wenn keine schnelle Diagnose und zeitnahe Behandlung erfolgen. Dieser Artikel beleuchtet die Pathophysiologie und die Behandlung traumatischer Zwerchfellhernien.
Chylothorax steht bei jeder Katze mit einem Pleuraerguss auf der Liste der Differenzialdiagnosen; in diesem Artikel erläutert Elizabeth Rozanski ihre bevorzugte Herangehensweise an diese Fälle.
Asthma ist eine häufige Erkrankung bei Katzen, kann aber zahlreiche andere Erkrankungen imitieren. Die Diagnose und die Behandlung können große Herausforderungen sein, wie uns dieser Artikel darlegt.
